- 综合治疗肉芽肿性乳腺炎45例
- 发布于 2013-04-12 09:29 来源:王颀医生
肉芽肿性乳腺炎(granulomatous mastitis,GM) 是非哺乳期乳腺炎的一种,又称肉芽肿性小叶性乳腺炎、哺乳后瘤样肉芽肿性乳腺炎、乳腺瘤样肉芽肿等。本病病因不明,多认为是一种自身免疫性疾病,与乳腺癌、导管周围乳腺炎及乳腺结核等易混淆,误诊误治,疾病迁延不愈,甚至导致全乳切除等不良后果。近年来我们对GM的诊治进行了研究,应用类固醇激素联合手术的治疗GM,取得良好效果,现报道如下。
病例与方法
1、临床资料
1.1一般资料
2011年06月至2012年6月期间我院诊治经病理检查诊断的GM 45例,患者均为女性,年龄18~48岁,中位发病年龄30岁。发病时间 4天~2年,中位发病时间2月,所有病例中,2例患者无婚育史,2例患者为妊娠期发病,19例患者曾出现哺乳不畅,1例患者曾口服避孕药物,余21例哺乳史不详,均无吸烟史。
1.2临床表现
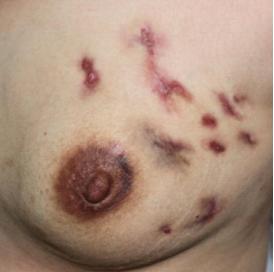
45例GM患者均主要临床表现为乳房肿块,单纯乳房肿块24例(53.3%),伴脓肿形成者21例(46.7%),其中2例患者曾在外院行脓肿切开引流手术,1例患者在广谱抗生素治疗期间脓肿自行破溃;有5例(11.1%)患者病损侵及皮肤和皮下出现覆盖皮肤的渐进性加重红斑或溃疡(图1a);合并乳头内陷者19例(42.2%);有2例患者在发病后在外院进行广谱抗生素治疗期间出现四肢关节红肿疼痛表现(图2a)。
1.3影像学检查
本组45例GM患者首次就诊均行乳腺超声检查,分级均为BI-RADS 4级,超声表现与乳腺癌相似,表现为单个或多个不规则形低回声区,边缘模糊,内部回声不均匀,CDFI 显示低回声边缘及内部均可见丰富的彩色血流信号。部分病例不规则低回声区潜行至皮下形成皮下及皮肤病灶(图3)。
有4例患者进行了乳腺X线检查(MG)为BI-RADS分级为0级,3-4级,主要表现为乳头后方腺体增厚,局部散在分布钙化,非对称性致密影及局部乳腺组织结构扭曲或紊乱等,41例患者因妊娠期、乳腺疼痛或脓肿形成等未行MG检查。
1.4病理诊断及细菌培养
所有病例均行空芯针穿刺(CNB)病理学检查,符合GM病理改变(图4a):以乳腺小叶单位为中心的肉芽肿性炎,可伴微小脓肿;小叶内有多种炎细胞浸润,包括中性粒细胞,单核细胞,淋巴细胞,上皮样细胞以及多核巨细胞(图4b)。伴脓肿者21例均行穿刺抽脓普通细菌培养,19(90.5%)例脓液细菌培养为阴性,2例(9.5%)为不典型细菌(普利茅斯沙雷氏菌和革兰氏阳性杆菌),所有病例均未发现抗酸杆菌生长。
2、治疗方法及效果
本组患者经血液检查、超声评估和病理确诊后,首先给予高剂量类固醇激素治疗:起始剂量甲泼尼龙片20mg/d,二周后症状缓慢可减量,通常每1-2周依次减量至16mg/d,12mg/d,8mg/d,4mg/d直至症状完全缓解或稳定,当病变可行手术切除时应及时手术,手术后减量至4mg/d用一周后可停药。原则上不用抗生素治疗。本组患者平均用药6.2周后病变完全缓解或肿块缩小至稳定可手术,5例伴皮肤损害的患者,皮损症状缓解(图1b)。
一般病灶缩小至2cm左右达到良好的手术条件时,行原发病灶切除手术,因切除缺乏病灶指引,不主张完全消失后才手术。切除范围包括肉眼可见的炎性病灶及皮损(图6),伴乳头内陷患者均同时行乳头内陷矫正术。经类固醇药物治疗后,病变缩小至不可扪及甚至复超声检查也可为阴性,但术中仍可见自乳头乳晕后腺体到乳腺外周分布的微脓肿和导管扩张等病灶(图5),且多聚集乳头乳晕后。2例患者为妊娠期患病,因妊娠期药物禁忌症,经CNB明确诊断后的妊娠期患者,均首先给予头孢呋辛口服治疗防止并控制急性症状,分娩后行类固醇激素治疗后手术。2例患者外院接受头孢类抗生素治疗期间出现骨关节疼痛及皮肤红斑,伴有血沉及C-反应蛋白升高等,均加大甲泼尼龙片起始剂量至28mg/d),骨关节疼痛及皮肤红斑在治疗1周内得到缓解(图2b),乳腺病变也渐好转,经激素治疗8周后,行区段切除术,手术范围包括皮损及炎症病灶。
3、 随访
所有病例随访5-12月,3例患者复发,其中1例患者为原手术部位复发,2例患者出现同侧乳房的非手术部位新发,1例患者因未遵循医嘱骤然停药出现反跳症状。以上4例患者均重新给予类固醇激素口服治疗,自20mg/d起始并缓慢减量,肿块减小后行手术治疗,手术范围包括病变累及的皮损,新发或复发病灶,随访至今,无复发。由于类固醇激素有加剧乳腺感染性疾病的可能,所以对于伴有急性症状的患者,给予激素治疗前应排除细菌感染性炎症,并给予广谱抗生素治疗,急性症状缓解后再给予类固醇激素。
讨论
GM首次是由Kessler 于1972年报道,该疾病好发于生育期经产妇女,大部分有哺乳不畅经历,患病年龄大多在20-50岁之间,但11岁和83岁患病的病例也曾有报道。GM病因学至今尚不明确,可能与自身免疫反应、高泌乳素血症、棒状杆菌感染等有关[ 1-4],发病机制可能是各种原因导致的乳汁淤积发超敏反应,表现为自身免疫反应的临床表现。本组有2例患者在治疗过程中出现骨关节疼痛及皮肤红斑,且血沉及C-反应蛋白升高等自身免疫反应表现,口服类固醇激素治疗后GM乳房病变及骨关节疼痛及皮肤红斑均得到明显改善。原发或继发高泌乳素血症在GM的发病机制中均起到重要的作用[ 2],哺乳期间泌乳素升高导致存留或外溢到乳腺导管中的脂肪或蛋白富集物引发的自身免疫性反应,口服避孕药及妊娠期女性GM也均有报道,而该疾病在未曾妊娠或哺乳的女性中较罕见。未经产女性的肉芽肿性乳腺炎血清泌乳素升高主要与垂体腺瘤、吩噻嗪所致高泌乳素血症、胃复安相关性乳溢相关。本组病例中2例患者无婚育史,2例患者为妊娠期发病,剩余41例患者中19例患者近3-5年曾有不良哺乳史,1例患者曾口服避孕药物,患者对类固醇激素有效,而抗生素无效。也有报道GM可能与棒状杆菌感染相关联,并分离出棒状杆菌[ 3 - 4],但此菌是条件致病菌。本组19例患者行脓液细菌培养,2例阳性,但未培养出棒状杆菌。GM有时会伴细菌感染,应用抗生素治疗急性症状改善后或同时给予类固醇激素治疗。
GM与导管乳腺周围炎(PDM)临床表现相近[ 5],都可以表现为肿块、脓肿、窦道或溃疡,一般抗生素治疗无效,术后反复发作,二者鉴别很重要,因两者治疗方法不同,GM的脓肿会引起皮损,如皮下肿脓、溃疡,本组5例(11.1%)患者侵及皮肤并出现覆盖于皮肤的红斑,部分红斑出现表皮溃破,破溃面为鲜红肉芽组织,痛感不明显,无异常分泌物;而PDM则是形成窦道,最后确诊还是空芯针穿刺活检[ 6]。影像学检查如乳腺超声及MG是用于排除乳腺癌等其它乳腺疾病的基础检查手段,也是GM患者随访中评估治疗效果的重要检查方法,但对GM和PDM的诊断帮助不大。与乳腺癌的鉴别一定要用经皮活检技术,不宜用针吸细胞学检查,容易误诊漏诊。本组45例病理均采用空芯针穿刺活检,组织病理学表现均符合GM的病理诊断标准,包括多核巨细胞,上皮样组织细胞浸润的肉芽肿性炎,偶伴有脂肪坏死。GM还应特别注意其它肉芽肿性疾病如乳腺结核,结节病,Wegener’s 肉芽肿病等鉴别。
GM的治疗仍存在争议[7,8],类固醇激素、甲氨蝶呤、抗生素及手术治疗等均有报道。少量文献报道GM应用抗生素治疗,但多数患者进展为蜂窝织炎,脓肿及窦道[9]。本组患者全部采用类固醇激素加手术综合治疗,GM伴急性感染症状及妊娠期GM患者2例先抗生素治疗控制急性感染症状后类固醇激素加手术综合治疗,均取得好的效果。我们认为类固醇激素加手术综合治疗是治疗GM的重要和有效的方法,重点是先用类固醇激素缩小病灶,手术尽量切除病灶和皮损,特别要注意乳头后方病灶的切除,保留正常组织。文献推荐剂量为泼尼松片2-30 mg⁄day,至少6周,并应持续用药至病变完全缓解[10],本研究应用甲基强的松龙片,起始剂量为20mg/d,病灶缓解后缓慢减量,通常每1周至2周减量4mg,顺序减量为16mg/d,12mg/d,8mg/d,4mg/d直至症状完全缓解或稳定,择机手术治疗后,甲基强的松龙片4mg/d维持3-7天后停药,本组患者平均用药6.2周后病变完全缓解或肿块缩小至稳定,达到良好的手术条件后手术,伴乳头内陷患者均同时行乳头内陷矫正术。本组病例随访5-12月,3例患者复发,本组复发率6.7%,其中1例患者为术后原发部位复发,2例为同侧乳房其它部位新发。1例患者自行停药出现激素骤停反跳症状,复发患者按上述治疗方法给予新一周期治疗,随访至今未复发。在类固醇激素治疗过程中,应注意药物副反应,包括皮质功能亢进综合症、加重感染、骨质疏松及股骨头坏死等。本组接受类固醇激素治疗的所有患者,均未出现严重副反应。
由于多数学者认为GM属自身免疫性疾病,故有学者发提出免疫抑制疗法,每周低剂量口服使用甲氨蝶呤、咪唑硫嘌呤长期治疗(6-12月),可有效缩短类固醇皮质激素使用的时间和剂量,有效减轻炎性反应过程,预防和减少皮质激素撤药后病情进展、窦道形成或复发[11]。2009年首次报道单药应用甲氨蝶呤治愈的2例肉芽肿性乳腺炎患者[12]。所以,对于不能耐受高剂量类固醇激素副反应的患者、激素治疗效果欠佳、激素停药后复发和病灶皮损溃疡广泛无法手术或要做全乳切除等难治性GM,我们开始尝试应用类固醇激素联合甲氨蝶呤免疫抑制疗法,已初见成效(图6a,图6b)。一般先类固醇激素常规治疗,减量后择机加甲氨蝶呤(10-15mg/w),类固醇激素减量至维持量,停类固醇激素则以病灶不加重为标准,同时服用叶酸,治疗期间需注意胃肠道、骨髓移植、肾脏损害等副反应。
总之,GM的诊断和治疗涉及多学科包括微生物学、病理学、影像学、免疫学及外科学等。我们推荐类固醇激素联合外科手术的综合治疗,可避免全乳切除并降低复发率,难治性GM可用类固醇激素加甲氨蝶呤免疫抑制治疗。