- 什么是食管癌?
- 发布于 2015-01-08 22:11 来源:胡旭东医生
在北美和欧洲食管腺癌是最主要的食管癌类型。胃食管返流性疾病(GERD)和肥胖是主要危险因素。目前已经知道的癌前损害是 Barrett 食管,通过内镜检查发现,发现后按照癌前损害进行治疗和监控。
亚洲、非洲、南美和北美的黑人食管鳞癌是食管癌主要类型。酒精和烟草是主要危险因素,食管鳞状异型增生是主要癌前损害。过去的 10 年里,尽管食管癌 5 年生存率仍然很差,但已有改善,早期和局部进展期食管癌病人长期生存可能性正在提高。
美国的 Anil Rustgi 和 Hashem B.EI-Serag 博士在 NEJM 上发表了一篇综述,主要讨论两种类型食管癌的流行病学和病理发生机制以及预防与治疗,重点强调近年的进展。
食管腺癌和食管鳞癌的流行病学
食管癌有两种主要类型,鳞癌和腺癌。虽然世界范围内食管鳞癌占所有食管癌 90%,但食管腺癌死亡率和发生率正不断提高,北美和欧洲几个地区已超过食管鳞癌。食管癌年轻人罕见,发生率随年龄增加而增长,发病高峰 70~80 岁。食管腺癌男性高发,是女性 3~4 倍,食管鳞癌男女没有差别。
美国预计 2014 年,新发食管癌病例 18,000 例,15,000 例死于食管癌。过去 30 年,食管鳞癌发生率正在下降,食管腺癌发生率正在逐渐提高(图 1)。
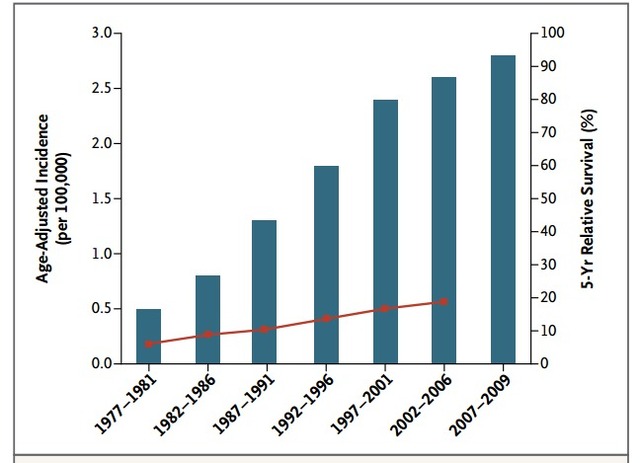
图 1. 食管腺癌发生率和生存率的倾向
环境危险因素
人群为基础病例对照队列研究显示 GERD、吸烟和肥胖是食管癌主要危险因素。若每周出现一次 GERD 症状,食管腺癌发生率增加,风险因子 5,若每天出现一次,风险因子增加到 7。大于 50 岁的人发展为食管腺癌的绝对风险大约是每年 0.04%。高达 40% 的食管癌病人没有 GERD 症状。
吸烟者发生食管腺癌风险是不吸烟者 2 倍,认为吸烟导致食管鳞癌发生风险高于食管腺癌,是食管鳞癌强风险因素。以人群为基础研究未揭示食管腺癌和酒精的关系。饮酒者食管鳞癌发生率是非饮酒者 3-5 倍,若同时伴吸烟,风险增加更明显。过多摄入肉类、脂肪和加工食物增加两种类型食管癌风险,多摄入纤维、新鲜水果和蔬菜降低风险。
食管腺癌发生率增加有如下假说,GERD 增多、肥胖 +GERD 增多、幽门螺杆菌感染减少。肥胖增加食管腺癌风险,风险因子 2.4~2.8,特别是腹部肥胖增加 Barrett 食管和癌症风险,可能是胃内压力增高致食管下段括约肌松弛,形成食管裂孔疝,共同促进加重 GERD。男性腹部肥胖常见,一定程度解释了癌症风险的性别差别。
有幽门螺杆菌感染的人群发生食管腺癌的风险降低。Meta 研究显示,有幽门螺杆菌感染病人食管腺癌风险减少 41%。幽门螺杆菌能导致胃炎,减少胃酸产生,降低食管上皮暴露于酸成分,减少 Barrett 食管和腺癌形成风险。大部分病例去除幽门螺杆菌后,没有产生或是加重 GERD。没有发现幽门螺杆菌和食管鳞癌之间明确的联系。
有报道食管腺癌与阿伦磷酸钠使用有关,然而进一步研究结论相互矛盾。人类乳头状瘤病毒可能增加食管鳞癌风险,但证据仍不充分。另外患食管运动疾病 - 弛缓不能的病人患食管鳞癌的风险增加 10 倍。
遗传风险因素
Barrett 食管和腺瘤具有家族群发性,基因组范围内联合种系相关分析在三个候选基因中鉴定出 11% 的 Barrett 食管和腺瘤具有胚胎突变,这三个候选基因是 MSR1、ASCC1 和 CTHRC1。
突变的 MRS1 同 cyclinD1 过度表达有关,导致快速的细胞周期进展。在另一项基因组关系研究鉴定出 Barrett 食管和腺瘤的易感位点,位于 CRTC1(编码 CREB 调节转录因子)、BARX1(食管特异性相关蛋白)和 FOXP1(食管分化相关蛋白)。
掌跖角化病,是一种罕见的家族性的食管鳞癌,常染色体显性遗传病,染色体 17q21-22 位点 RHBDF2 错义突变,该基因编码失活菱形酶。基因组关系研究已经鉴定出中国食管鳞癌患者一系列易感位点,这意味着食管鳞癌是复杂的基因和环境相互作用有关。
一项最近研究,分析了食管腺癌患者正常组织和癌组织中全外显子测序中的突变谱,共发现了 28 个突变基因,其中五个与腺癌的发病机制有关,他们是 TP53、CDKN2A、SMAD4、ARIS1A、PIK3GA。
食管腺癌中这些基因和分子途径的改变非常普遍。种系特异性因子,特别是转录因子,在食管癌的发生中非常重要。中国食管鳞癌病人的全基因组和全外显子测序发现了 8 个突变基因,6 个是已知肿瘤相关基因,2 个是新发现的基因。
食管癌动物模型
现在已经建立了几种食管癌动物模型。啮齿类手术动物模型,胃切除后行食管空肠吻合或食管十二指肠吻合,诱导胆汁反流,再现 Barrett 食管和肿瘤进展。具有 P120 连环蛋白的小鼠模型,该蛋白通常用于稳定细胞膜上的 E-cadherin,如果该蛋白被去除就会导致食管鳞癌。
还有食管腺癌的遗传性模型。例如食管特异性 EB 病毒 L2 启动子与白介素 1-beta 融合,诱导炎症因子微环境,诱导 Barrett 食管形成。该小鼠饮用水中加入胆酸,或是与另一种 P16 肿瘤抑制基因缺失小鼠杂交,加速食管腺癌发生。
另一种方法就是敲除 P63 基因,该基因对鳞状上皮干细胞或前体细胞的增殖非常关键,最终导致 Barrett 样的细胞群向鳞柱交界细胞转化。
三维立体细胞培养“器官型培养”是对动物模型的补充,用来阐明 Barrett 食管发生发展路径。Barrett 食管中可能存在干细胞或前体细胞的转化导致重新编程,或是鳞状食管基底细胞分化,或是胃贲门细胞转化。Barrett 食管细胞出现后,损害内可出现异型增生和恶性肿瘤。三维器官型培养模型已经用于研究食管鳞状细胞癌。
内镜检查与监测
认为 Barrett 食管是食管腺癌前体,分化的肠道柱状上皮细胞代替了正常的鳞状上皮。大型队列研究结果显示,对没有异型增生的 Barrett 食管病人每年癌症风险是 0.12~0.40%。Barrett 食管损害中如果存在异型增生明显增加患癌风险,低级别异型增生每年发生癌症风险 1%,高级别异型增生患癌风险超过 5%。
80~90% 食管腺癌没有 Barrett 食管。持续 GERD 病人中 6~12% 内镜检查发现 Barrett 食管,多数是超过 50 岁白人男性。无异型增生 Barrett 食管推荐每 3 年一次内镜。尽管缺乏随机直接证据,大多数观察研究认为内镜监测 Barrett 食管发现腺瘤时,早期患癌可能性更大,应接受根治性治疗,比因有症状才诊断治疗的病人生存时间更长。
除了能够早期检测癌症。对有低级别或高级别异型增生的 Barrett 损害进行射频消融治疗可使 77% 病例食管化生缓解,86% 异型增生缓解、进展风险降低,患癌更少。长期随访已经证实了这些作用的持续性,但是射频消融治疗后持续监测是有必要的,因为会出现复发,最常见的复发是非异型增生,内镜可以治疗。
现在指南不推荐内镜消融治疗非异型增生 Barrett 食管,若 Barrett 食管较长、严重 GERD、Barrett 食管或腺癌家族史的高危病人应考虑消融治疗。癌前病变治疗通常是个体化的,不考虑经济效益比。尽管也有其它 Barrett 食管进展生物标志,但没有任何一个能象内镜这样清楚地显示异型增生且如此精确。
食管鳞癌的前期损害是食管鳞状异型增生。具有轻度、中度或重度异型增生病人,发生鳞状细胞癌风险逐渐提高,风险因子分别为 3、10 和 30。中国部分地区,食管癌检查方法包括内镜或细胞刷检,这些方法也是有价值的,推荐用于弛缓不能或是碱性溶液摄入导致食管狭窄,目前尚无指南推荐此类病人的诊治。
预防
质子泵抑制剂
第一项观察性研究显示,质子泵抑制剂治疗减少 Barrett 食管病人出现高级别异型增生和腺癌风险。但这些研究存在不足,譬如选择偏倚、未对共因子作调整。一些回顾性研究显示,患 GERD 或 Barrett 食管癌病人经抗反流手术后,未减少食管腺癌发生风险,该手术不推荐单纯用于癌症预防。
阿司匹林和非甾体类抗炎药
观察性研究显示阿司匹林和非甾体类抗炎药能降低食管腺癌和鳞癌风险 40~50%,推荐用作普通高危人群癌症预防手段。但一项随机试验显示塞来昔布治疗不减少 Barrett 食管和低级别 / 高级别异型增生患者患癌风险。另一项随机研究显示塞来昔布不影响食管鳞状异型增生进展。目前就此正做进一步研究。
他汀类药物
一项分析显示他汀类药物使用者同非使用者相比,减少食管腺癌发生风险 28%,减少 Barrett 食管腺癌发生风险 41%。然而这些研究的不一致性非常明显,包括剂量、持续时间或他汀药物类型。
将人口统计学研究结果转化为实际的预防推荐虽然符合逻辑,但缺少证据,不像禁烟,减肥、调整饮食结构的证据如此明确。中国进行的预防试验显示,营养补充,如维生素和矿物质,不能减少癌前损害,也不降低发生率或死亡率,在食管癌、普通人群或食管鳞状异型增生人群中都是如此。
食管癌的临床表现
食管腺癌和食管鳞癌的人口统计学和风险因素不同,但临床表现相似,内镜表现也相似,但大约 3/4 腺癌出现在远端食管,而鳞状细胞癌经常出现在近或中段食管。
常见临床表现包括进行性吞咽困难、体重减轻、烧心对药物治疗无反应和失血表现。较少出现的症状包括声音嘶哑、咳嗽、返神经受损相关肺炎或侵犯气管支气管。患有头颈部鳞状细胞癌的病人患食管鳞癌风险增加。
治疗
表1对食管癌的治疗进行了总结,两种组织类型食管癌治疗通常相似,但在化疗与手术治疗的选择上有几点不同,胃食管结合部腺癌通常认为是食管腺癌的延伸。
表1、食管腺癌的治疗
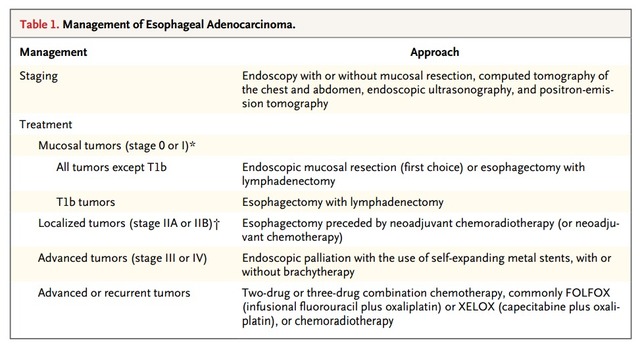
分期
食管癌预后与治疗依赖精确评估癌症侵犯深度和淋巴结侵犯情况(图2)。过去十年里,内镜超声和 PET 检查已经改善了分期,内镜超声对肿瘤和淋巴结状态评估精确性可达 70~80%,内镜超声基础上加入细针活检进一步改善淋巴结分期敏感性。胸腹部图像检查未发现明显局部或远处播散者,内镜超声检查对分期特别有帮助,内镜黏膜切除,能进一步改善分期,增加治愈机会。
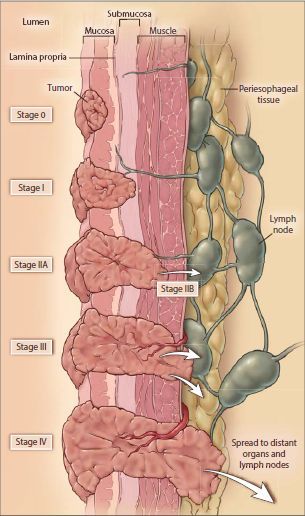
图2、食管癌分期
PET 检查用于鉴别隐匿的远处转移,通常在锁骨上或后腹膜淋巴结,10~20% 的病例因为 PET 检查的发现而划分为进展期。
黏膜肿瘤
当 Bsrrett 食管内高级别异型增生或腺癌只局限于粘膜上皮层内时,伴或不伴有消融的内镜黏膜切除是近年来治疗上的主要进步,特别是小肿瘤,这些小肿瘤通常无症状,而且没有环周切换缘。如果 Barrett 食管仍未完全消失,可以加做内镜消融。
淋巴结转移的风险与肿瘤侵犯深度有关。伴高级别异型增生的 Barrett 食管,淋巴结侵犯风险几乎为 0,I 期肿瘤淋巴结侵犯风险为 1~2%。没有随机试验比较内镜治疗和手术治疗,几项观察性研究显示两种方法治愈率和生存率相似。
对 0 期或 I 期且无禁忌症或合并症的腺癌病人,内镜治疗应当首选。对肿瘤已经侵犯到粘膜肌层并进入粘膜下层的 T1b 肿瘤,淋巴结转移风险高达 20%,根治性食管切除是优先选择方法,但一些治疗中心扩大了内镜治疗适应症,其中就包括低风险的黏膜下肿瘤。
局部进展期肿瘤
局部进展期肿瘤定义为 T3N1,最佳治疗手段是食管切除,虽然也有研究显示单独根治性放化疗也能达到治愈,特别是鳞状细胞癌病人,但这种方法没有随机对照试验的证据支持,所以应当只限于病人状况下降,或健康情况不足以耐受食管切除。
单纯食管切除术与高复发率有关,5 年生存率很低 5~34%。近年对需要食管切除术病人的治疗进展是进行新辅助放化疗或化疗。随机对照试验显示,和单纯手术相比,新辅助化放疗或化疗可使两种类型食管癌都有生存获益。卡铂结合紫杉醇或是顺铂结合氟尿嘧啶类化放疗在美国正在成为标准治疗,在欧洲单纯新辅助化疗是优先选择方法。
新辅助化放疗的优势只是比单纯化疗略多一点点。Meta 分析显示,新辅助化放组,全因死亡风险比 0.78,新辅助化疗组 0.87,腺癌获益超过鳞状细胞癌。手术前后皆接受化疗对鳞状细胞癌患者获益略有增加。
除了对切除标本进行组织学检查外,没有其它可信任的检查能证实新辅助治疗的反应性,所以食管切除非常有必要。腺癌、有残留、淋巴结阳性病人,尽管新辅助治疗后行完全切除,结果仍很差,而辅助化疗或放化疗对此类病人是否获益不清楚。辅助化疗用于淋巴结阳性鳞状癌,此方法在几个日本随机试验中已经显示获益。
较大的医学中心或是有经验的手术医生,手术结果看起来更好,术后合并症发生率与治疗明显获益。胸腹两个区域淋巴结切除术在大多数欧洲和北美医学中心是标准术式,一些国家还切除颈部淋巴结,因为颈部淋巴结常受鳞癌侵犯。微创食管切除手术的安全性和合并症与标准食管切除术相似,但这项技术很具挑战性。
进展期肿瘤
无法切除的食管癌导致阻塞症状,通过内镜下食管支架或大剂量腔内照射解决。内镜放置自充式金属支架是解决吞咽困难一线选择。自充式金属支架同局部治疗相比,症状缓解率更高,较少处理合并症。内置支架基础加入大剂量内照射,能适度延长生存。其它治疗如内镜扩张或消融、塑料支架、旁路手术或放化疗不推荐,因有效性低和较高合并症。
为了延长生存,姑息性化疗也经常用于治疗不能切除的、转移或复发的食管癌。卡铂或是顺铂联合氟尿嘧啶或是卡培他滨,反应率 35~45%,延长生存几个月,特别是鳞状细胞癌。三种药物联合可能增加 5~10% 反应率,但伴有更高毒性。
二线化疗仍处于研究中,非选择性病人采用吉非替尼作为二线治疗不能改善总生存。多西他赛联合 ramucirumab 治疗比较有前景。曲妥珠单抗增加进展期食管腺癌总生存和无进展生存分别为 2.7 个月和 1.7 个月。
预后
美国食管腺癌病人 5 年总生存 17%,较鳞癌 5 年生存率略高。手术治疗病人总生存和无进展生存明显改善。尽管检测早期食管腺癌能力不断提高,大多数肿瘤仍是出现区域或远处转移时才发现,5 年生存率由局部食管癌 39% 下降到远处转移食管癌的 4%。而且 60~70% 的食管癌并没有得到指南推荐治疗。多学科讨论能够改善食管癌治疗。
总结
食管腺癌的主要风险因素是 GERD、肥胖和吸烟,幽门螺杆菌感染降低食管癌发生风险。吸烟、喝酒是食管鳞癌主要风险因素。内镜检查能鉴别 Barrett 食管,定期监测 Barrett 食管以发现异型增生和早期食管腺癌。
内镜消融是有效治疗异型增生的方法,也是粘膜内腺癌治疗的主要手段。对基因组区域和基因进行甄别,有助于发现食管癌潜在发病机制,并有助于发现新的生物标志和发展新的治疗手段。
