- 会么是黄斑裂孔?
- 发布于 2012-02-10 16:02 来源:赵明威医生
(一)、疾病简介
黄斑裂孔是指黄斑部视网膜内界膜至感光细胞层发生的组织缺损,严重损害患者的中心视力。Knapp和Noyes分别于1869和1871年最早报导了外伤性黄斑区视网膜裂孔,Kuhnt于1900年首次报导非外伤性黄斑裂孔,此后,各种原因的黄斑裂孔相继被认识。
该病的患病率不高,约占人群的3.3‰,其中以不明原因的特发性黄斑裂孔最为多见(大约83%),常发生于50岁以上的健康女性(平均65岁,女:男=2:1),双眼患病者占6%~28%。也有部分发生在较年轻的患者。
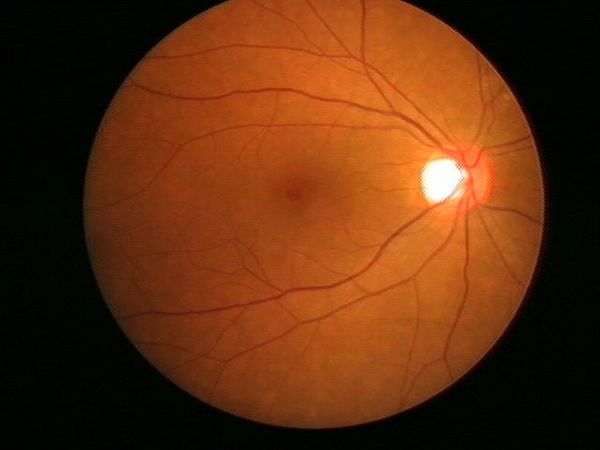
图1 特发性黄斑裂孔 彩色底图
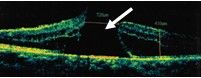
图2 特发性黄斑裂孔 OCT扫描图
(二)、疾病分类
1、根据病因分类:
(1)特发性黄斑裂孔
(2)外伤性黄斑裂孔
(3)高度近视黄斑裂孔
(4)其他继发性黄斑裂孔
2.、根据黄斑裂孔的形态
(1)全层黄斑裂孔
(2)板层黄斑裂孔
(三)、发病原因
除特发性黄斑裂孔外,其它原因所致者病因均较明确,如外伤、高度近视、囊样黄斑水肿、炎症、视网膜变性类疾病、黄斑前膜和日蚀性视网膜病变等。
对特发性黄斑裂孔的认识则经历了一个多世纪的漫长时光,直至1988年Gass提出了黄斑区视网膜表面切线方向的牵拉是特发性黄斑裂孔形成的主要原因,为采用玻璃体手术治疗黄斑裂孔提供了理论基础。该理论的提出,是基于玻璃体视网膜交界面的比邻解剖关系得出,在人体的老龄过程中,由于玻璃体液化和发生玻璃体后脱离。使视网膜表面常残余部分玻璃体后皮质,由于这些残余后皮质中的玻璃体细胞发生增值,在黄斑中心凹区视网膜表面形成平行于视网膜表面的牵张力,最初发生黄斑中心小凹脱离,继而发生中心凹脱离,最终形成黄斑全层裂孔。
(四)、发病机制
有关黄斑裂孔的发病机制尚不完全清楚。最早期的文献报导认为外伤是黄斑裂孔形成的主要原因,然而随着病例报导的增加,人们发现仅约5%~15%的黄斑裂孔为外伤引起。本世纪初,有作者提出囊样黄斑变性是黄斑裂孔的主要发病原因,也有人认为年龄相关性血管改变导致黄斑萎缩而最终形成黄斑裂孔,但这些观点都不能解释特发性黄斑裂孔的发病机制。1924年,Lister首次提出玻璃体牵拉与黄斑裂孔形成密切相关,自此,人们开始注意到玻璃体在黄斑裂孔发病时所起的重要作用,并逐渐认为玻璃体对黄斑区视网膜的纵向牵拉是黄斑裂孔的发病原因。1988年,Gass对特发性黄斑裂孔的发病机理提出了革命性的见解,认为黄斑中央凹前的玻璃体切线方向牵拉是特发性黄斑裂孔形成的主要原因,为采用玻璃体手术治疗黄斑裂孔提供了理论基础(图31-3)。此后,有关玻璃体切割手术治疗黄斑裂孔的报导不断增多。通过玻璃体切割,特别是剥除玻璃体后皮质和视网膜前膜,松解玻璃体黄斑牵拉,使大部分病例裂孔闭合,某些病例术后视力明显提高。1995年,通过临床病理研究以及根据玻璃体手术后视力可以提高这一事实,Gass进一步指出,特发性黄斑裂孔形成过程中不伴有中央凹视网膜神经组织丧失,从而解释了为什么手术后视力能够恢复。
(五)、病理生理
黄斑裂孔的临床病理可表现为①黄斑孔大小400~500μm。② 黄斑裂孔周围“脱离”范围达300-500μm。③ 感光细胞发生萎缩。④ 黄斑囊样改变。⑤ 类似于玻璃膜疣的黄色点状沉着物附着于RPE表面。⑥ 出现视网膜前星形细胞膜。
(六)、临床表现
(一) 症状 该病起病隐匿,常在另一只眼被遮盖时才被发现。患者常主诉视物模糊、中心暗点、视物变形。视力一般为0.02~0.5,平均0.1。
(二) 眼底表现与临床分期 根据特发性黄斑裂孔形成过程中不同阶段的眼底表现,Gass将其分为四期(图31-4):I期:起病初期,黄斑中央凹前玻璃体皮质自发收缩,引起视网膜表面切线方向牵引,导致中央小凹脱离,眼底中央凹反光消失,中央凹区视网膜色素上皮(RPE)表面出现黄色小点(100~200mm),此时为Ia期;中央凹前玻璃体皮质进一步收缩,黄斑中央凹脱离,RPE表面出现黄色环(200~350mm),此时为1b期。Ia与1b期均不伴有玻璃体与黄斑中央凹的分离,亦未出现“真正的”全层黄斑孔,临床上称为先兆黄斑孔(impending macular hole),视力轻度下降至0.3~0.8,荧光素眼底血管造影可显示黄斑中央凹轻微的高荧光。

图 3 特发黄斑孔I 期
II期: 起病数日~数月后,玻璃体切线方向进一步牵拉,在中央小凹边缘形成黄斑裂孔,逐渐扩大,由新月形发展至马蹄形,最后形成圆形裂孔,常伴有盖膜。少数情况下,黄斑孔于中央凹中央开始形成,逐渐扩大后变为无盖孔。最近研究发现,在特发性黄斑裂孔形成过程中并没有视网膜中央凹组织丧失,所谓的“裂孔前盖膜”是浓缩的玻璃体后皮质。黄斑裂孔周围可见视网膜下液边缘,裂孔处有黄色玻璃膜疣状沉着物,视力下降至0.1~0.6。荧光素眼底血管造影可呈中度高荧光。

图 4 图3 患者发展为II 期黄斑孔
III期:以上病变经2~6个月后,由于视网膜组织收缩,黄斑裂孔扩大至400~500μm,伴或不伴有盖膜,此时为III期黄斑孔。可见黄色玻璃膜疣状沉着物与视网膜下液边缘,中央小凹周围囊样改变,视力下降至0.02~0.5。
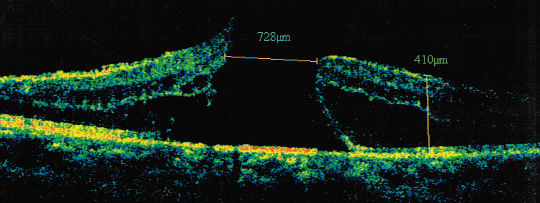
图 5 特发黄斑孔III 期
IV期:早期表现为黄斑孔盖膜前移位,晚期表现为玻璃体与黄斑、视神经乳头的完全分离,此时为4期黄斑孔。
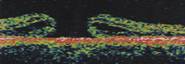
图 6 特发黄斑孔IV 期
(三)自然病程
I期黄斑孔(先兆孔):约50% 发展为全层黄斑孔,50%的病例在玻璃体与黄斑中心凹分开后自发缓解。
II期黄斑孔:多数病例于2~6个月后发展至3期孔。多数病例黄斑孔大小发展至400mm以上。
III期黄斑孔:少于40%的病例发展至VI期黄斑孔。80%病例视力相对稳定。通常于1年后视网膜脱离区RPE脱色素,半年后即可出现色素分界线。很多病例出现视网膜前膜。偶然发生视网膜自发复位,也可发生视网膜脱离。
(四)对侧眼
(1) 玻璃体与黄斑中央凹分离:无黄斑孔形成危险。
(2) 玻璃体与黄斑中央凹未分离:黄斑孔形成可能性<15%。
(3) 黄斑前膜覆盖中央凹区,常伴有黄色小点:黄斑孔形成可能性<1%。
(4) 黄斑中央小凹前星形混浊伴视网膜放射状皱褶:无黄斑孔形成危险。
(5) 如黄斑区出现黄色点或环,且合并先兆黄斑孔的其它表现,表明具有形成黄斑裂孔的高度危险。
(七)、诊断要点
自从眼底相干光断层扫描(OCT)问世以来,黄斑孔诊断已无困难。当眼底镜检查发现黄斑区可疑破孔时行OCT扫描即可确定诊断。
(八)、鉴别诊断
1、病因鉴别:需除外特发性黄斑裂孔以外的致病原因,如外伤、炎症、高度近视、囊样黄斑水肿、眼底血管病、变性类疾病、日蚀性视网膜病变等导致的继发性黄斑水肿。
2、形态鉴别:应与另外2种玻璃体牵引性黄斑病变鉴别。
(1)特发性黄斑前膜:有时合并黄斑裂孔,眼底及OCT检查均可明确诊断。
(2)玻璃体黄斑牵引综合征:常导致黄斑牵引变形、黄斑水肿,有时与黄斑裂孔同时存在。OCT检查可确诊。
(3)板层黄斑裂孔:OCT检查可明确黄斑裂孔是否为全层或板层。
(4)黄斑裂孔性视网膜脱离:常发生于高度近视,特发性黄斑裂孔常在黄斑裂孔周围出现孔源翘起的浅脱离晕,但极少发生真正意义的视网膜脱离。
(九) 、治疗原则和进展
1、黄斑孔的手术治疗以前是一个禁区,只有在有较大范围的周围视网膜脱离时才考虑。近年来由于对黄斑孔发病机理的研究认识到黄斑孔的形成与玻璃体对黄斑中心凹切线方向的牵引密切相关。因此广泛开展了用玻璃体切割的方法切除中心凹前的玻璃体皮质治疗黄斑孔。
手术目的为缓解玻璃体黄斑牵拉,对I 期患者,切除玻璃体特别是去除黄斑区前的玻璃体后皮质可使已脱离的黄斑中央小凹复位。对已形成全层黄斑孔的患者,手术目的则是多方面的,包括缓解玻璃体黄斑牵拉、剥离与黄斑孔发病相关的黄斑前膜或视网膜内界膜、眼内气体填塞以使黄斑孔闭合等。对于难治性黄斑裂孔(如:大孔或复发孔),使用自体血清、β2转化生长因子(TGF-β2)或自体浓缩血小板涂抹于黄斑孔上可能增加孔区的脉络膜视网膜粘连,促使孔封闭愈合。
2、适应证
(1) 治疗性玻璃体切割术:目的在于促使黄斑裂孔闭合及裂孔周围视网膜浅脱离复位。
A、明确诊断为II~IV期特发性黄斑裂孔,视力明显下降(0.05~0.4)、有明显的视物变形者。
B、黄斑裂孔形成时间在一年以内,愿意接受手术者。
(2) 在Gass对黄斑裂孔的分期中, I期黄斑裂孔并未形成全层黄斑孔,约1/2患者I期黄斑裂孔可自发缓解,所以多不主张对I期黄斑裂孔进行手术,对具有发展为全层黄斑孔的高危患者可慎重选择手术。
玻璃体切割是否可以预防全层黄斑裂孔形成尚无定论。美国一项多中心、随机、对照临床研究结果,对于I期黄斑裂孔患者,玻璃体切割组与未手术观察组比较,全层黄斑裂孔发生率分别为37%和40%(P=0.81),由于所观察病例数尚少,目前还不能肯定预防性手术的疗效。因此,拟行预防性玻璃体切割手术治疗I期黄斑裂孔需权衡利弊,手术的“利”为缓解玻璃体对黄斑的机械牵拉,而“弊”则为手术可能带来的风险,包括:手术操作可能引起全层黄斑裂孔、周边视网膜医源性裂孔、视网膜脱离、感染、晶状体混浊等。
3、手术方法及进展
传统手术技术为标准三切口经睫状体平坦部玻璃体切割术,行人工玻璃体后脱离,次全切除玻璃体,剥离黄斑前膜或黄斑区视网膜内界膜,或辅以生物制剂封闭黄斑孔。用20%~25%的SF6气体行膨胀气体/空气交换。术毕,患者俯卧位约14天后,玻璃体腔内气体吸收,恢复正常体位。
(1) 微切口玻璃体手术
2002年,25G经结膜无缝合玻璃体切割手术系统问世。2003年,23G无缝合玻璃体切割系统被用于玻璃体手术。目前,这两种玻璃体切割设备已被应用于特发性黄斑孔手术中。国内赵明威等提出采用20G手法小切口玻璃体手术也取得良好效果并降低了手术成本。
(2) 内界膜染色技术
内界膜剥除多使用内界膜染色技术,染色剂有台盼蓝(trypan blue),亮蓝G(brilliant blue G, BBG),溴酚蓝(bromphenol blue,BPB),芝加哥蓝(Chicago blue, CB),曲安奈德(triamcinolone,TA)以及吲哚菁绿(indocyanine green,ICG)等。曲安奈德不能使内界膜着色,但可以使其变得容易辨认。
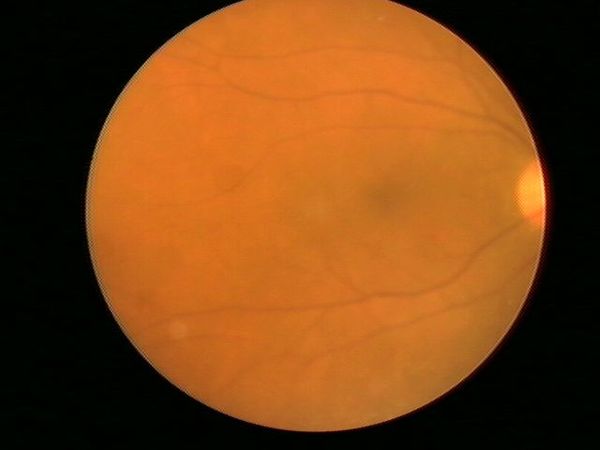
图7 图1患者术后,黄斑孔闭合,黄斑中心凹形态恢复
4、手术并发症
治疗特发性黄斑裂孔的手术并发症与普通玻璃体切割手术的并发症相似,包括核性白内障、一过性高眼压、医源性视网膜裂孔产生、黄斑裂孔扩大、光毒性引起的视网膜色素上皮病变、血管阻塞以及眼内炎等。其中核性白内障的发病率最高,可达12%-90%,文献报道约33%的病例在首次手术后5~16 个月需要进行白内障摘除和人工晶体植入术,在黄斑裂孔闭合眼,视力恢复到玻璃体手术前的视力或更好。约17.4%的手术眼发生一过性高眼压,多发生在术后3周内,主要由气体填充所致,一般对症治疗即可。手术当中尽量避免医源性视网膜裂孔的产生,如果出现医源性裂孔,应尽可能采用激光封孔取代冷凝封孔,以降低黄斑前膜等术后并发症的发生。
(十)、手术评估及预后
黄斑裂孔视力损失的主要原因有以下几点 ① 裂孔处无视网膜感光细胞。② 裂孔周围视网膜浅脱离。③ 裂孔周围囊样水肿。④ 裂孔周围视细胞不同程度变性。通过玻璃体切割手术松解裂孔前后方向以及切线方向的牵拉,从而消除病因;通过气体填充和生物因子使黄斑裂孔闭合,促使视网膜神经上皮复位,因而可以改善视力及视物变形等症状。
对于采用不同手术方法治疗黄斑裂孔的疗效,不同的研究结果不尽相同。Kelly(1991)等单纯使用玻璃体切割术(52例),裂孔闭合率为58%,视力提高2行以上者为42.3%,2年后该作者的病例累积达170例,此时的裂孔闭合率为73%,视力提高2行以上者为55%。近年来研究发现,在手术中使用自体血小板、自体血清、转化生长因子β2 (transforming growth factor β2,TGF-β2)、纤维蛋白原等填充于黄斑裂孔内,可增加裂孔处脉络膜视网膜粘连愈合,并有效地提高视力。文献报道,使用玻璃体切割联合TGF-β2封闭黄斑裂孔的裂孔闭合率为91%~100%,视力提高2行以上者83%~90.1%,但也有术者未能重复出相同结果,并发现术后眼压升高反应明显。最近Thompson 等报导,使用TGF-β2与安慰剂对照比较,二者在黄斑裂孔的解剖复位与视力改善方面并无显著差异。Gaudric(1995)等首先报导使用自体浓缩血小板封闭黄斑裂孔,并用单纯玻璃体切割作对照(各20例),结果血小板组裂孔闭合率为95%,视力提高2行以上者为85%,而单纯玻璃体切割组裂孔闭合率仅为65%。近年来随着手术技术的不断进步,越来越多的证据表明,单纯使用玻璃体切割联合内界膜剥除即可获得较高的手术成功率。Christensen等人[10]的一项随机对照临床试验结果表明,对于2期与3期特发性黄斑孔,内界膜剥除后黄斑孔封闭率显著高于不剥除内界膜组(2期黄斑孔,100%比55%,3期黄斑孔,91%比36%)。
影响手术预后的因素有如下几点:① 裂孔是否闭合。 裂孔闭合差者视力恢复不满意。术后裂孔是否完全闭合,可能与术中黄斑前玻璃体后皮质是否清除干净、裂孔周围的膜是否剥除、裂孔周围是否还有张力以及与患者术后头位保持有关。② 术后并发症的出现对视力恢复亦有影响,如白内障形成,发生医源孔时经巩膜冷冻后出现视网膜前增生膜等。③ 术中在黄斑孔区操作时注意避免对黄斑区视网膜组织的器械损伤。
随着OCT技术的进展,人们对特发性黄斑孔预后的认识也不断加深。Inoue等人[11]使用频域OCT对53例术后黄斑裂孔闭合的患者进行检查,发现光感受器内节与外节的连接可能对黄斑孔术后视力恢复起重要作用。术后内外节间连接缺损越严重,视力预后越差。随着时间发展,某些患者内外节间的连接可以部分恢复,而在另外一些病人则持续存在。
(十一)、疾病预防
对于存在明确病因的非特发性黄斑裂孔,可通过治疗原发病以及密切随诊检查预防黄斑裂孔的发生。特发性黄斑裂孔目前尚无有效预防方法。
(十二)、疾病护理
黄斑裂孔手术由于眼内填充气体的缘故,术后需俯卧位,俯卧持续时间取决于眼内填充的气体种类。一般为1-2w。此时按玻璃体手术后眼内填充护理常规进行护理。








