- NOTES经肛全直肠系膜切除术
- 发布于 2010-09-01 23:49 来源:陈远光医生
-
作者注:本文报告我们2010年5月21日应用国际上直肠癌最新术式“NOTES经肛全直肠系膜切除”治疗一例男性直肠癌的情况,可能是因为该术式创新性较强,2010年8月27日在苏州举行的“中华医学会第十二届全国腹腔镜与内镜外科会议”安排作者作了大会自由发言。该术式的意义在文中有讨论,在此不再赘述。
NOTES经肛内镜直肠癌全直肠系膜切除
陈远光 胡明 雷建 陈家诚 李娟云广州医科大学附属第一医院普外科陈远光
广州医学院第一附属医院胃肠外科
广州市沿江路151号 510120
电子邮箱 chenyggz@yaho.com.cn
摘要
背景和目的 全直肠系膜切除已成为世界性的直肠癌手术金标准,其传统方法无论是开腹或在腹腔镜下进行,均经前腹壁进行。2007年以来有研究经肛自然腔道手术切除直肠和乙状结肠。2010年5月国际上首次报告为一例女性直肠癌患者按照全直肠系膜切除原则进行经肛内镜切除。本文首次报道2010年5月该新手术在一例合并左侧游走肾的男性直肠癌患者的应用。
方法 该例男性患者,47岁,合并左侧盆腔游走肾以及盆位阑尾,术前临床分期为CT3Nx,行新辅助化疗后肿瘤直径由3cm缩小到1.5cm。手术初分两组分别进行,拟腹组经腹腹腔镜辅助分离直肠上端和乙状结肠及其系膜以及肠系膜下血管,肛组游离直肠系膜。但腹组因为左侧盆腔游走肾的干扰未能寻得肠系膜下血管,后由负责肛组的术者交替完成两组操作。术者在PPH肛门镜下横断直肠壁后先完成腹组以上操作,再进行肛组操作,通过自制的腰形直肠镜按照TME原则向上分离直肠系膜直至从骶前间隙进入腹腔。进入腹腔后,因为精囊腺的阻碍,盆底腹膜前部的分离困难,即经前腹壁腹腔镜下进行。确认乙状结肠游离的长度足够后,经肛门直肠镜将直肠和乙状结肠拖出,切断乙状结肠并用吻合器行直肠和乙状结肠吻合。
结果 手术时间4小时50分,直肠系膜完整切除并检出 25 个淋巴结,其中5个直肠下部系膜淋巴结阳性,直肠及其系膜的远切缘均阴性,最后病理分期 pT3N2 。术后患者恢复顺利,第二天开始口服肠内营养,第五天和第八天分别开始半流饮食和普通饮食。未发生吻合口漏和感染,第七天后排便功能接近正常。
结论 自然腔道手术经肛内镜全直肠系膜切除可行而安全,腹腔镜辅助有助于克服精囊腺和游走肾造成的分离困难 。
关键词 自然腔道手术 全直肠系膜切除 腹腔镜 直肠癌 游走肾 经肛
NOTES Transanal Endoscopic Total Mesorectal Excision For Rectal Cancer
Yuanguan Chen,Ming Hu,Jian Lei,Jiacheng Chen,Juanyun Li
Department of Gastrointestinal Surgery, 1st Affiliated Hospital of Guangzhou Medical College
510120,Number 151,Yanjiang Road,Guangzhou City,China
e-mail: chenyggz@yahoo.com.cn
Abstract
Background Total mesorectal excision(TME) has become the worldwide gold standard for rectal cancer,its traditional laparotomy or laparoscopic procedure is performed through the anterior abdominal wall.Since 2007, Natural OrificeTranslumenal Endoscopic Surgery (NOTES) transanal endoscopic rectosigmoid resection has been studied in human cadavers and porcine models. The first clinical report of a woman patient of NOTES transanal endoscopic rectal resection with TME for rectal cancer using laparoscopic assistance was published in May 2010.We first report the new procedure applied on a man patient with rectal cancer and left ectopic pelvic kidney in May 2010.
Methods The patient was a 47-year-old man with a CT3N0 rectal cancer combined with left ectopic pelvic kidney and pelvic appendix ,the tumor had a diameter of 3 cm before and 1.5 cm after neoadjuvant chemotherapy , his body mass index (BMI) was 22 kg/m2. Transabdominal laparoscopic dissection of the rectosigmoid and the inferior mesenteric vessels was planned to be performed synchronously with transanal endoscopic mobilization of mesorectum at first,but searching for the inferior mesenteric vessels was puzzled by ectopic pelvic kidney and it was too difficult for abdominal team to do, then the operator who was in charge of transanal procedure finished both transabdominal and transanal dissection in turn. The rectum was transected through PPH anoscope at first and then the above abdominal dissection was finished, the mesorectum was mobilized upwards to peritoneal cavity with the TME principles through a self-made wraist-shape proctoscope. After entering the peritoneal cavity from the presacral plane, the forepart of pelvic floor peritoneum was hindered by the seminal vesicle, and was dissected under transabdominal laparoscope. After confirming that sufficient length of sigmoid colon had been mobilized,the rectosigmoid was exteriorized transanally,and the specimen was transected transanally followed by staped colorectal anastomosis.
Results The operative time of was 4 hours and 50 minutes. Mesorectal excision was complete,25 lymph nodes were retrieved from the specimen,and the final pathology demonstrated pT3N2 with 5 positive nodes of lower mesorectum and negative margins of distal rectum and mesorectum. The patient recovered smoothly . Enteral nutrition ,semi-liquid diet and normal diet was taken respectively on the second, fifth and eighth postoperative day. No anastomotic leakage and infection was encountered, nearly normal defecation came back on the seventh postoperative day.
Conclusions NOTES transanal endoscopic TME in man patient for rectal cancer combined with ectopic pelvic kidney is feasible and safe. Laparoscopic assistance is helpful to overcome difficulties caused by left pelvic ectopic pelvic kidney and seminal vesicle.
Keywords Natural orifice translumenal endoscopic surgery,Total mesorectal excision , Laparoscopy , Rectal cancer, Ectopic pelvic kidney , Transanal
0 引言
全直肠系膜切除(Total mesorectal excision,TME)由Heald于1982年首先报告提出,是近年来直肠癌外科最重要的进展,现在已经成为世界性的金标准[1-4]。传统的TME无论是开腹或在腹腔镜下进行,均经前腹壁进行,为分离和取出标本所需,常要做或大或小的腹壁切口,由此可导致感染、出血、伤口疼痛、远期形成疝等风险和并发症。为消除这些切口并发症,自2007年以来,有研究在猪模型以及人尸上经肛自然腔道手术(Natural OrificeTranslumenal Endoscopic Surgery ,NOTES)尝试切除直肠和乙状结肠,发现这种无腹部切口的方法可行,而且可以经肛完成TME[5-11]。2010年5月国际上首次报道为一例女性直肠癌患者按照TME原则进行NOTES经肛内镜切除[12]。
但是,迄今为止,未见在男性直肠癌患者按照TME原则进行NOTES经肛内镜切除的报道,故无从得知男性患者手术的特点。本文首次报道为一例男性直肠癌患者进行该新手术。有趣的是该患者同时患有左侧游走肾。
1 临床资料和手术方法
术者有传统TME、经肛手术治疗直肠脱垂和先天性巨结肠等方面的经验。实行该例新手术前,手术团队以猪为模型进行了成功的动物实验,新手术也取得了医院审批同意和患者的知情同意。为避免盆腔游离肾的潜在不利影响和缩短手术时间,术前讨论中设计经前腹壁腹腔镜下处理腹内的直肠乙状结肠及其系膜以及肠系膜下血管,经肛内镜下处理腹外直肠及其系膜。
1.1 临床一般资料
该男性患者47岁,体重指数22kg/m2,既往无重大疾病史,因便血两周经肛门指检和直肠镜检发现直肠左前壁肿块,距离肛缘5cm,病理活检为中分化腺癌。经FOLFORI方案新辅助化疗三个周期后,肿瘤直径由3.5 cm缩小到1.5 cm, 术前盆腔MRI提示直肠旁脂肪间隙浸润明显减轻,系膜内未见明显肿大淋巴结,胸片、腹部CT未发现转移, CEA 2.0 ng/ml,临床分期为CT3NxM0。
1.2 术前准备
术前一天下午口服复方聚乙二醇行肠道准备。手术开始前静脉应用头孢菌素预防感染。全麻后留置导尿管和中心静脉导管。截石位,直肠用安尔碘灌洗消毒。
1.3 手术方法
1.3.1 经前腹壁腹腔镜观察探查
经脐下Veress针穿刺建立气腹,压力12 mmHg,然后置入10mm套管和腹腔镜,经右下腹置入10mm套管作主操作孔,左下腹及耻骨上置入5mm套管为辅助操作孔。腹腔镜下未发现肝脏以及其他器官转移,盆腔无粘连,但是左侧盆腔肾将乙状结肠和上段直肠及其系膜向前向上向右侧推移,同时阑尾盆位附着于直肠右侧壁上。探查后初腹组和肛组同时开始操作,但是因为腹组游离盆腔阑尾后,未能克服游离肾造成的困难寻得肠系膜下血管。随后由计划中负责肛组操作的术者交替完成两组操作。
1.3.2 经肛内镜游离直肠系膜
PPH肛镜插入肛门并缝合固定于肛周皮肤,直肠壁切断线设计为V形, 肿瘤侧距离肛缘3 cm 对侧为 4 cm。切断线粘膜下注射美蓝标记后先作一荷包缝合封闭直肠腔,然后用超声刀全层切断直肠壁,切断后未见系膜脂肪即进入前列腺直肠间隙(图1)以及骶前间隙。直肠横断后其远断端环形收缩,妨碍操作,约向上游离直肠系膜2 cm后,操作极为困难,即取出肛镜换用自制腰形直肠镜(专利申请中)。此直肠镜长8cm, 腰部中央直径4 cm,上端直径5.5 cm,使用时肛门被扩张固定于腰部中央,远端直肠被扩张固定于腰部上方之外,不再妨碍操作。从此镜自下向上按照TME原则在盆筋膜脏层壁层之间的无血管区进行分离,由骶前间隙进入腹腔(图2),注意勿损伤前列腺精囊腺以及骶前血管。进入腹腔后,精囊腺后坠填满直肠镜前半视野,致使分离盆底腹膜前部困难,即将腰形直肠镜用手套封闭,转由腹腔操作切断盆底腹膜前部。
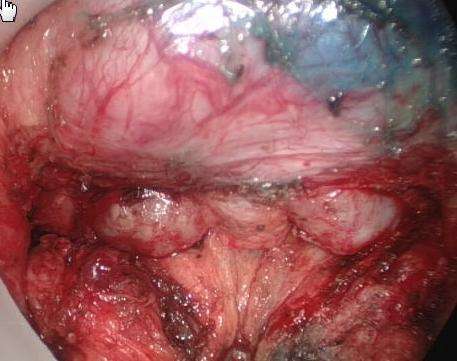
图1. 经肛直肠镜下进入前列腺直肠间隙
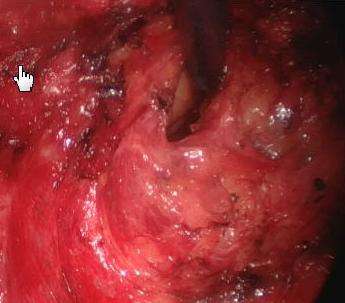
图2.经 肛直肠镜下经骶前间隙进入腹腔
1.3.3 经前腹壁腹腔镜分离
因为盆腔游走肾的干扰,腹腔镜下未能见到常规内侧入路标志――腹主动脉分叉,仔细观察后,术者发现直肠和乙状结肠内侧系膜边缘仍然隐约可见,只是被推移到右侧数厘米,即自右侧髂动脉下方开始沿系膜边缘自下而上分离系膜直到根部,系膜血管根部裸化后在左结肠动脉下用可吸收夹夹住后用超声刀切断。游离乙状结肠其余系膜,向乙直交界上方5cm处肠壁放射状切断之,向下游离直肠系膜到腹膜返折水平中止,经肛内镜完游离腹膜返折下直肠系膜从骶前进入腹腔后,再经腹腔操作切断盆底腹膜前部。腹腔镜镜下确认乙状结肠长度足够吻合,将乙状结肠直肠标本装入塑料袋内经直肠镜从肛门拖出。
1.3.4 结直肠吻合
肛门外于乙直交界上方5cm处切断乙状结肠,近断端内置入吻合器砧后回纳入腹,重新置入PPH肛镜,盆底置一引流管从肛旁引出,直视下予直肠远断端荷包缝合,用32号圆形吻合器行结肠直肠端端吻合。肛内置入肛管引流,肛管头端置于吻合口上约10cm处。最后,行吻合口渗漏试验,未发现渗漏。
2 结果
2.1 术中过程及所见
经PPH肛镜下易行全层横断直肠壁,也易进入前列腺直肠间隙以及骶前间隙。肛镜下直肠壁的远断端收缩成环,初期妨碍了向上游离直肠系膜,但是后期可以利用便于荷包缝合。用腰形直肠镜可以将直肠壁远断端收缩环扩张置于镜外,由此建立的操作空间足以进行直肠系膜游离,不必应用TEM平台充气建立操作空间。经肛游离直肠系膜可以达到腹膜返折水平, 该水平上的游离因为游走肾和精囊腺的妨碍须由经腹的腹腔镜完成。手术总时间为4小时50分。
2.2 术后病理及恢复情况
直肠周围的盆筋膜脏层除右侧精囊腺附近有长1.5cm的裂口外余处均完整(图3)。标本上共检出25个淋巴结,最后病理报告直肠中分化腺癌浸润肠壁全层,下部系膜内8个淋巴结中5个有转移,肠壁切缘以及系膜切缘均阴性。
患者术后恢复顺利,第二天始预口服场内营养, 第五天第八天分别开始半流和普通饮食;肛旁引流管在术后初有少量血性液体引流出,数小时后引流液即转为黄色清亮,量少;无吻合口漏和感染出现,第三天始肛门排气排便,第五天拔除肛旁引流管,一周后排便功能接近正常。术后腹壁外观满意(图4)。
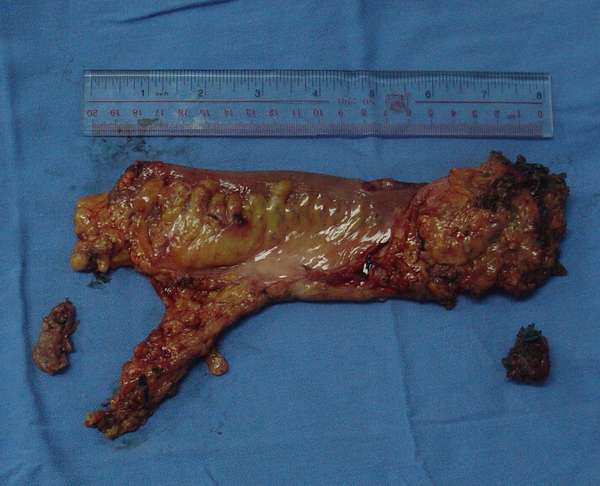
图3 切除标本

图4 术后腹部外观
3 讨论
NOTES经肛内镜TME扩大了NOTES的适应症,能既根治直肠癌又取得腹壁无切口的微创和美容效果[5-12]。与Sylla 等[12]施行的第一例女性手术一样,本例合并盆腔游走肾的男性直肠癌的手术过程显示,NOTES经肛TME在男性也为可行,肿瘤学方面的满意效果以及无吻合口漏和感染等提示其是安全的新手术。
游离直肠系膜时,传统的开腹或腹腔镜TME,经前腹壁进入腹腔,自上往而下从腹膜反折附近开始到直肠远切端附近结束,其操作空间较大,层次容易辨认;而NOTES经肛TME与传统TME顺序刚好相反,操作空间较小,层次是否容易辨认?系膜能否完整?这是关系到其是否可行的关键问题。与文献[12]报道一致,本例手术显示经PPH肛镜下易行全层横断直肠壁,也易进入前列腺直肠间隙以及骶前间隙,系膜切除完整,初步提示NOTES经肛TME可行。
自从2005年报道第一例临床上NOTES经胃镜切除阑尾以来,经胃和阴道手术的研究远远超过经结肠和肛门手术的研究,这主要是因为后者存在粪便污染腹腔导致术后感染的可能性;就NOTES经肛内镜直肠乙状结肠切除而言,最近研究不支持这种感染的可能性[7,12]。本例也未发生感染。其原因可能是,感染的发生不仅与细菌污染有关,而且与污染的程度和抗污染的措施有关。就NOTES直肠切除而言,充足的术前肠道准备、手术前肠内消毒、近切端以上的肠段从手术开始即予封闭、远切端以下肠段极为短小靠近体外易于消毒、术后适当的盆底引流,可以使手术区域有污染而无感染。
文献报道的实验多以雌猪为对象,首次临床应用也是在女性患者身上进行[6,7,10-12]。作者在临床应用前曾经以公猪为对象进行实验,发现经肛游离直肠系膜进入腹腔后精囊腺后坠妨碍视野和操作,在此例临床应用中也发现相同现象。这种困难在本例是通过腹腔镜辅助操作得以克服。是否有更佳办法如应用软镜尚待进一步研究。另外,本例合并盆腔游走肾,不能按照腹腔镜下常规内侧入路标志寻得肠系膜下血管,但是仍然可以沿着隐约可见的直肠乙状结肠内侧系膜边缘分离直到根部,经腹的腹腔镜视野宽大便于观察,提示异常解剖下可以通过复合的腔镜内镜技术解决困难,不必拘泥于应用一种方法如单纯NOTES。
与传统的剖腹和腹腔镜TME相比, NOTES 的TME消除了腹部切口及相应的并发症[5-12]。与NOTES 的经胃和阴道等其他途径相比,经肛途径的TME具有特殊优点。第一,经肛途径可以最大限度地既根治又保留肛门功能,因为该法可以在肛镜直视下切断直肠,必要时可以在手术开始就行直肠远端切缘的快速病理切片检查确定有无癌残留。第二,经肛途径创伤最低,缘于其他途径接近肿瘤需通过正常健康组织,而经肛途径通过的是治疗需要切除的组织,而且经肛途径游离腹膜返折下的直肠系膜可以不需要免充气,如与经腹操作同步进行尚可缩短手术时间。第三,经肛途径适应者最多,无性别差异,因为这种方法无需切开阴道,男女均适用。第四,经肛途径更经济,因为可以在肛镜直视下予远切端荷包缝合,不需要双吻合器技术,降低了医疗费用。第五,该法易于学习和掌握,胃肠外科或普外科医生不仅可以采用其所熟悉的常规腹腔镜器械和技术进行操作,而且可以借鉴类似手术经验,如Parks手术、直肠肿瘤经肛局部切除、经肛手术治疗直肠脱垂和先天性巨结肠、PPH 、全腹腔镜TME标本从直肠拖出等;而经胃途径和经阴道途径或需重新学习胃镜操作技术或需妇科医生协助。
当然,NOTES经肛TME也有天然的局限和缺点。例如术中较长时间的扩张对肛管功能必然有一定影响;如果低位肿瘤体积大而盆腔空间狭小,从肛内向上游离直肠必然困难重重。本例因为游走肾的存在而采用了经腹的腹腔镜辅助,术前化疗成功使肿瘤明显缩小,故对以上影响难以评判。本例为个案,有关的肿瘤治疗的长期效果有待观察。
因此,结合文献,从本例成功的经验来看,经肛门NOTES的TME这种新的手术方法可行而安全,较其他NOTES的途径具有更多的优点和吸引力。腹腔镜辅助有助于克服精囊腺和游走肾造成的分离困难。但应用这种方法治疗直肠癌,尚需要更多的研究以严格评估适应症和禁忌症,并解决一些技术和器械上的难题。
4 参考文献
1.Heald RJ, Husband EM, Ryall RD. The mesorectum in rectal cancer surgery--the clue to pelvic recurrence?Br J Surg. 1982;69(10):613-6 [PMID: 6751457]
2. Heald RJ, Ryall RD. Recurrence and survival after total mesorectal excision for rectal cancer. Lancet. 1986;1(8496):1479-82[ PMID: 2425199]
3.陈远光, 陈道瑾, 金钦文, 吴君晖, 钱立元.直肠上动脉灌注美蓝指导全直肠系膜切除. 世界华人消化杂志 2003;11(1):117-119
4.雷建,陈远光,黎绍基.直肠癌全直肠系膜切除术研究进展.广州医学院学报2004;14(04):83-87
5.Whiteford MH, Denk PM, Swamstrom LL. Feasibility of radical sigmoid colectomy performed as natural orifice translumenal endoscopic surgery (NOTES) using transanal endoscopic microsurgery. Surg Endosc.2007; 21:1870C1874 [PMID: 17705068]
6. Sylla P, Willingham FF, Sohn DK, Gee D, Brugge WR, Rattner DW. NOTES rectosigmoid resection using transanal endoscopic microsurgery (TEM) with transgastric endoscopic assistance: a pilot study in swine. J Gastrointest Surg 2008;12(10):1717C1723.[PMID: 18704596]
7. Sylla P, Sohn DK, Cizginer S, Konuk Y, Turner BG, Gee DW,et al. Survival study of NOTES rectosigmoid resection using transanal endoscopic microsurgery with or without transgastric endoscopic assistance in a swine model. Surg Endosc. 2010; 24(8):2022-2030[ PMID: 20174948]
8. Ricardo Zorron. Natural orifice surgery applied for colorectal diseases. World J Gastrointest Surg 2010; 2(2): 35-38
9. Fajardo AD, Hunt SR, Fleshman JW, Mutch MG. Video. Transanal single-port low anterior resection in a cadaver model. Surg Endosc. 2010;24(7):1765 [ PMID: 20054571]
10.Trunzo JA, Delaney CP.Natural orifice proctectomy using a transanal endoscopic microsurgical technique in a porcine model. Surg Innov. 2010;17(1):48-52[PMID: 20097670]
11.Tan KY, Maeda T, Konishi F.Multimedia article. Transanal endoscopic resection of the rectum with high ligation on a swine model--a novel type of natural orifice endoscopic surgery. Dis Colon Rectum. 2009 Dec;52(12):2045-7 [PMID: 19934929]
12. Sylla P, Rattner DW, Delgado S, Lacy AM. NOTES transanal rectal cancer resection using transanal endoscopic microsurgery and laparoscopic assistance.Surg Endosc. 2010;24(5):1205-10. [PMID: 20186432]
