- 胰腺神经内分泌肿瘤诊治指南
- 发布于 2015-02-16 13:14 来源:王成医生
胰腺神经内分泌肿瘤 ( pancreatic neuroendocrine neoplasms,pNENs),原称为胰岛细胞瘤,约占原发性胰腺肿瘤的 3%。依据激素的分泌状态和患者的临床表现,分为功能性和无功能性胰腺神经内分泌肿瘤。
无功能性 pNENs 约占 75%~85%;功能性 pNENs 常见的有胰岛素瘤和胃泌素瘤,胰岛素瘤一般位于胰腺,而胃泌素瘤多见于十二指肠或胰腺;其余的功能性 pNENs 均少见,统称为罕见功能性胰腺神经内分泌肿瘤 ( rare functional pancreaticneuroendocrine tumors,RFTs),包括生长抑素瘤、胰高糖素瘤,生长激素瘤等;功能性 pNENs 约占 pNENs 的 20%。
大部分 pNENs 是散发和无功能性的,多因肿瘤局部压迫症状或体检时发现,部分因肝脏及其他部位的转移,进一步检查发现原发 pNENs 病灶。功能性 pNENs 常表现为激素相关的症状,如低血糖、多发性消化性溃疡、腹泻等,临床上通常较早发现。
少部分 pNENs 是遗传性神经内分泌肿瘤综合征的表现之一,如多发性神经内分泌肿瘤Ⅰ型 ( multiple neuroendocrine neolasia I,MEN-I) 和 Von Hippel-Lindau 综合征,这类患者一般较年轻,家族中或本人也有其他神经内分泌肿瘤的病史。
pNENs 临床表现多样,诊疗措施较复杂且周期较长,建议在多学科协作模式下进行,由胰腺外科、内分泌科、影像诊断科、内窥镜、肿瘤内科、介入科、病理科和护理等专业人员共同参与,并贯穿患者诊治的全部过程。根据患者的基础健康状况、激素分泌相关临床症状、肿瘤分期、分级等信息,以循证医学为基础,个体化地应用多学科及多种治疗手段,以使患者达到最佳的治疗效果。
一、pNENs 的分期和分级
(一)pNENs 的分级
按组织分化程度和细胞增殖活性进行分级。增殖活性分级推荐采用每高倍镜下核分裂象数和(或)Ki-67 阳性指数两项指标,分级标准见表 1。

(二)pNENs 的分期
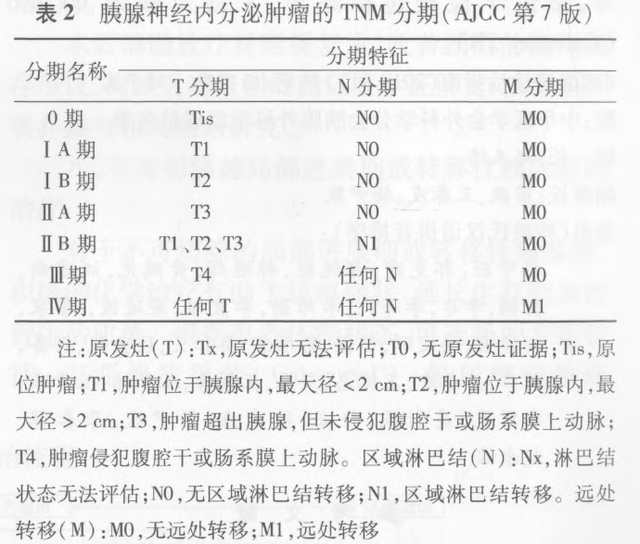
推荐采用 AJCC 2010 年发布的第七版 pNENs 的 TNM 分期(表 2)。
二、pNENs 的术前诊断
pNENs 的术前诊断包括定性诊断和定位诊断。定性诊断即明确病变的性质,穿刺活检是常用的手段,但对可切除胰腺肿瘤,不要求术前一定取得病理学证据。pNENs 常用的血清学指标有嗜铬粒蛋白 A(chromogranin A,CgA) 和神经元特异性烯醇化酶(neuron specific enolase,NSE),异常升高提示有神经内分泌肿瘤的可能。
依据激素分泌的相关症状和血清激素的水平,可判断功能性 pNENs 的功能状态,并指导对激素相关症状的对症治疗。
影像学检查如增强 CT 和 MRI 对 pNENs 有重要的诊断价值,多表现为动脉相早期强化的富血供病灶。对 pNENs 的手术治疗来说,定位诊断是关键步骤,除了可明确原发肿瘤的部位外,还可以同时评估肿瘤周围淋巴结的状态及是否有远处转移。
定位检查常见的手段有:
(1) 胰腺增强 CT 和(或)MRI;
(2) 内镜超声检查;
(3) 生长抑素受体显像和 68G-PET-CT;
(4) 经皮经肝穿刺脾静脉分段取血;
(5) 动脉造影;
(6) 术中超声。
三、pNENs 的手术治疗
手术是 pNENs 的主要治疗手段,也是目前唯一可能治愈 pNENs 的方法,手术的目的是争取 RO 切除。
(一)局部可切除 pNENs 的手术治疗
1、胰岛素瘤和<2 cm 的无功能性 pNENs,可考虑行肿瘤摘除术或局部切除术。>2 cm、或有恶性倾向的 pNENs,无论是否有功能,均建议手术切除,必要时可包括相邻器官,并清扫区域淋巴结。胰头部的 pNENs 建议行胰十二指肠切除术,亦可根据病灶大小、局部浸润范围等行保留器官的各种胰头切除术;胰体尾部的 pNENs 应行远端胰腺切除术,可保留或联合脾切除;位于胰体的肿瘤可行节段性胰腺切除术。
2、对于可切除的局部复发病灶、孤立的远处转移灶或初始不可切除的 pNENs,经综合治疗后转化为可切除的病灶时,如果患者体力状况允许,应考虑手术切除。
3、偶然发现的≤2 cm 的无功能 pNENs,是否均需手术切除尚有争议,应根据肿瘤的位置、手术创伤的程度、患者年龄、身体状况和患者从手术中的获益,衡量利弊做出选择。
(二)局部进展期和转移性 pNENs 的手术治疗
局部不可切除 pNENs 的影像学评估和标准参照胰腺外科学组的《胰腺癌诊治指南 (2014)》。目前认为,减瘤术或姑息性原发灶切除不能延长患者的生存,但在下列情况下可考虑施行:
(1) 局部晚期或转移性 G1/G2 级无功能 pNENs 患者,为预防或治疗出血、急性胰腺炎、黄疸、消化道梗阻等严重危及生命和生活质量的并发症,可行姑息性原发灶切除术。
(2) 功能性 pNENs 的减瘤术:对功能性 pNENs 患者,减瘤手术(切除 >90% 的病灶,含转移灶)有助于控制激素的分泌,缓解激素过量分泌的相关症状。减瘤术时应尽可能保留正常的组织和脏器。
(3) 无功能性 pNENs 的减瘤术:对无功能转移性 pNENs,如仅存在不可切除的肝转移灶,原发灶切除可能有利于对肝转移灶的处理,可考虑原发灶切除。
(三)家族性神经内分泌肿瘤综合征患者胰腺病灶的处理
对于合并 MEN-I 和 Von Hippel-Lindau's 综合征的患者,因其胰腺内常存在多个病灶,术前需仔细判断手术时机以及手术方式。术中需结合超声检查,尽可能发现所有病灶。推荐施行远端胰腺切除 + 胰头部的病灶剜除术,以尽量保留一部分胰腺功能。
(四)胆囊切除术
进展期 pNENs 患者手术后,若需要长期接受长效生长抑素治疗,建议在手术时同时切除胆囊,以减少患胆汁淤积和胆囊炎的风险,尤其是原来已经合并胆囊结石的患者。
四、pNENs 切除的术前评估和准备
(一)术前评估
需排除遗传性综合征如 MEN-I、Von Hippel-Lindau 综合征,这些遗传病需要特殊的术前准备、治疗和随访策略。术前应仔细评估原发灶,如肿瘤局部侵犯的范围、与周围脏器的关系、淋巴结转移情况、是否存在远处转移和激素的分泌状态。重要的是评估患者接受手术的风险获益比,制定个体化的手术计划。
依据神经内分泌肿瘤的自然病程及生长相对缓慢的生物学行为,如手术的风险超过获益,应放弃手术切除。术前应检查血清 CgA 和 NSE,血清 CgA 水平的变化可反应肿瘤的转移、复发;对预后也有重要的预测价值;NSE 对 G3 级肿瘤的随访有重要价值。
(二)术前准备
pNENs 手术除常规的术前准备外,有不同于其他胰腺手术之处:对功能性 pNENs 患者,术前应检测血清激素水平,并控制激素过量分泌引起的症状;如采用葡萄糖滴注控制胰岛素瘤的低血糖;质子泵抑制剂控制胃泌素瘤的腹泻和溃疡出血;生长抑素控制血管活性肠肽瘤的腹泻和水电解质失衡;胰高糖素瘤患者容易形成血栓,可采用小分子肝素抗凝。
合并类癌综合征的患者在麻醉前,需静脉输注短效生长抑素,防止出现类癌危象。
五、晚期 pNENs 的综合治疗
(一)pNENs 肝转移的治疗
1、肝脏是 pNENs 最容易出现远处转移的部位,如果手术能切除绝大部分转移灶除(> 90% 的病灶),可考虑原发灶和肝转移灶同期或分期切除。如肿瘤位于胰头部,建议先作肝转移灶切除,然后二次手术切除胰十二指肠。拟行肝转移灶切除时,应满足以下条件:
(1) 分化好的 G1/G2 肿瘤;
(2) 无远处淋巴结转移和肝外转移、无弥漫性腹膜转移;
(3) 无右心功能不全。肝转移灶切除的患者 5 年生存率为 47%―76%,高于未切除者的 30%~40%,但切除后的复发率可达 76%,且多于 2 年内复发。
2、射频消融、动脉栓塞化疗、选择性内放射治疗等局部治疗手段可用于控制肝转移灶,有效减轻肿瘤负荷,减少激素分泌,从而改善患者的生活质量。目前尚无前瞻性临床研究证明针对肝脏的局部治疗可改善患者的预后,但在临床实践中,这些局部治疗通常会与全身治疗联合应用。
3、肝移植:肝移植是治疗 pNENs 肝转移的手段之一,但指征需严格掌握。肝移植的指征是 pNENs 伴不可切除的肝脏多发转移灶,无肝外转移和区域淋巴结转移;原发灶可完整切除,活检肿瘤 Ki67<< span="">10%(Ki67<5% 预后更好);存在无法用药物控制的、影响患者生活质量的症状;无肝移植禁忌证。
(二)转移性 pNENs 的药物治疗
1、生长抑素类药物:生长抑素类药物治疗 pNENs 的客观有效率不到 10 %,但疾病控制率可达 50%~60%。大量回顾性研究以及前瞻性随机研究表明,生长抑素类药物可用于进展缓慢的 pNENs(G1 级和 G2 级)和生长抑素受体阳性的 pNEC(G3 级)的治疗,且不良作用较小。
2、分子靶向药物:前瞻性临床研究研究表明舒尼替尼和依维莫司对晚期和转移性 pNENs 具有较好的疗效及耐受性。舒尼替尼是多靶点酪氨酸激酶抑制剂;依维莫司是口服的 mTOR 抑制剂,二药均可显著延长 pNENs 的无肿瘤进展生存期。
3、化疗:链脲霉素联合 5-FU 和(或)表阿霉素治疗 Gl 级和 G2 级 pNENs 的证据最为充分,客观有效率为 35%―40%。近期的小样本、回顾性研究提示,替莫唑胺单药或联合卡培他滨对转移性 pNENs 也有一定疗效。5-Fu 或卡培他滨联合奥沙利铂或伊立替康等方案也可以作为 pNENs 二线治疗的选择。
六、术后随访和辅助治疗
(一)术后随访
所有的 pNENs 都具有恶性潜能,所以应该进行长期随访。对于根治性切除术后的 pNENs,建议每 6―12 个月随访 1 次,随访 10 年,若出现症状随时复查。对于未手术切除的低危患者,第 1 年应每 3 个月随访 1 次,以后每半年随访 1 次,至少 3 年,之后每年 1 次。
有远处转移的 pNENs 患者,应每 3―6 个月随访 1 次,接受治疗的患者随访时间应相应缩短。pNEC 患者按照导管腺癌的随访要求进行。随访内容至少应包括血清 CgA 和 NSE;影像学检查如 CT 或 MRI 检查,对于表达生长抑素受体 2a 的 pNENs 也可联合生长抑素显像进行随访。
(二)辅助治疗
目前尚无高质量的循征医学证据支持 R0 或 Rl 切除术后长效生长抑素、化疗或分子靶向药物等辅助治疗能使 pNENs 患者获益,故不推荐对根治术后的 G1 和 G2 级患者常规给予辅助性药物治疗;对有肿瘤复发高危因素的患者,如淋巴结转移、血管内癌栓,切缘阳性,可考虑开展辅助治疗的临床研究。对于根治术后的病理报告为 G3 级的患者,可按照导管腺癌的治疗原则给予全身辅助治疗和(或)局部治疗。



