- 胰十二指肠切除胰肠吻合方式的一点改进
- 发布于 2015-02-15 10:58 来源:王刚成医生
胰肠吻合是胰十二指肠切除术中的关键环节之一,胰十二指肠切除术后腹腔引流管的出血、胰漏与胰肠吻合密切相关,胰肠吻合的操作及方法直接影响整体手术的时间及术后患者的恢复。经过多年外科学者探讨及临床总结,胰腺粘膜与空肠粘膜对接吻合作为胰肠吻合主要方式之一,在临床得到广泛应用。但胰腺粘膜与空肠粘膜对接吻合操作方法临床多种多样,没有统一的标准,操作不当,可能延误手术时间或导致局部组织出血及其它组织的副损伤影响胰肠吻合口愈合,笔者近几年采用分离式环形连续缝合行胰腺残端包埋、胰腺粘膜与空肠粘膜对接吻合,认为该缝合方法手术视野暴露充分,术中不易伤及其它组织,操作简便,缝合时间快、术后吻合口漏及吻合口出血发生率低。报告如下。
资料与方法
一.一般资料
2010年3月至2014年10月,胰十二指肠切除术胰肠吻合43例,其中男24例,女19例;年龄36~78岁,中位年龄62.5岁。其中,单纯胰十二指肠切除术32例,胰十二指肠联合右半结肠切除6例,胰十二指肠联合远端胃切除4例,胰十二指肠联合右肾切除1例。术前腹部CT、MRI检查及术中探查43例肿瘤未侵及肠系膜上血管及下腔静脉,无远处转移。所有患者均行肿瘤根治性R0切除,消化道重建采用Child法。胰肠吻合采用胰腺粘膜与空肠黏膜对接吻合,缝合方法采用分离式环形连续缝合。所有患者术前血生化、血常规、胸片、心电图、免疫检查,均无手术绝对禁忌;近期无急性发作全身感染,无激素内分泌类和 (或)影响免疫功能等药物服用史。均在气管内插管、静脉复合麻醉下由同一组医师行腹部开放手术。
二.胰肠吻合手术方法
⑴.游离空肠。距离屈氏韧带约25 cm用切割闭合器离断空肠,空肠残端加固封闭,距残端4.0 cm纵形切开空肠浆膜层,利用组织钳将浆膜层向两边与黏膜层分离,分离宽度与胰腺残端厚度相当,所暴露的空肠粘膜中间开一个直径约3mm小孔。⑵.胰腺残端止血及胰管内支撑管放置。胰腺残端用2-0可吸收线严格缝扎止血,将取去针头输液管10cm作为胰管内支撑管(根据胰管内径选择支撑管),支撑管一端剪2-3个侧孔,置入胰管并固定于胰腺残端。⑶.分离式行缝合胰腺残端与空肠吻合。取“4-0”缝线(w-8557普里灵)先自胰腺残端后壁进针出针后(避开肠系膜上静脉),再从空肠吻合口后壁浆肌层进针出针,胰腺残端与空肠间隔大约20cm(以术中不影响缝合操作为恰当距离),如此循环,连续缝合胰腺残端后壁与空肠后壁,针距相隔3mm, 后壁全部穿针完毕,收紧缝线,将胰腺内置管穿透空肠黏膜层进入空肠肠腔,空肠黏膜紧贴于胰腺残端表面,将胰腺残端前壁与空肠浆膜层前壁连续如缝后壁那样缝合,缝合胰腺一周后,首尾线打结固定。缝合完毕后,视针距给予间断缝合加强。
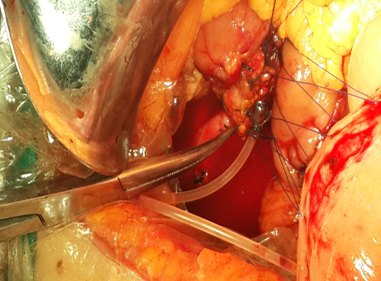
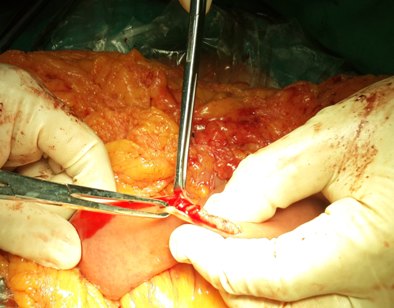
图1空肠浆肌层与粘膜层分离图2胰腺后壁与空肠浆肌层分离式连续缝合
三.胰漏判断标准
根据Bassi[5]等胰腺手术后胰漏诊断标准:术后3天及以上,腹腔引流液淀粉酶测定值大于正常,血清淀粉酶测定值上限3倍;可分为3级:I级,仅有腹腔引流液淀粉酶升高,无相应症状和体征;Ⅱ级,腹腔引流液淀粉酶升高,伴有典型临床症状,并开始出现器官功能不全征兆,需使用抗生素、营养支持及腹腔引流;Ⅲ级,患者病情严重.出现败血症和器官功能障碍,甚至可导致死亡,常需手术干预。
四.引流管引流内容物性状临床表现
存在胰漏的引流管内容物,颜色通常为灰褐色,较稠,无异味,如同合并感染脓样液体,引流物实验室细菌培养无细菌生长。未存在胰漏的引流管内容物表现为淡黄色液体,清亮。
结果
一 .术后围手术期患者临床恢复情况
根据胰漏判断标准,本组43例患者, 38例无胰漏,区域引流管无异常,术后腹部CT提示:胰肠吻合口附近无积液;4例为I级胰漏,引流管引流液淀粉酶值均高于正常值,区域引流管引流液呈淡黄,微混,无疼痛发热症状,术后腹部CT提示:胰肠吻合口附近无明显积液。1例为II级胰漏合并胆漏,腹腔引流管胰液淀粉酶值为10307u/L,区域引流管引流液呈黄白色,明显浑浊,每天引流液约400ml余,右肋缘下轻度按压疼痛,术后腹部CT提示:胰肠吻合口、胆肠吻合口周围积液。I级胰漏给与生长抑素持续应用3~5天,保持区域引流管通常引流,余未作特殊处理。II级胰漏给与生长抑素持续应用12天,增强场外营养支持,根据术后腹部积液位置,CT引导下置入相应引流管,保持无腹腔积液,术后21天后,腹腔引流管明显减少,患者一般情况良好,每天引流液100ml余,带管出院。43例患者胰肠吻合口出血0例,胰肠吻合时间为8~10分钟(吻合时间以连续缝合开始至吻合结束)。
2.术后病理:胆总管下段癌10例,胰头癌6例,壶腹部癌12例,十二指肠间质瘤5例,胃癌4例,结肠肝曲癌6例。
讨论
1.胰肠吻合方式及操作的重要性。胰肠消化道吻合方式从来就是外科学界探讨的焦点和重点,胰肠消化道吻合操作快慢直接影响全程手术时间,胰肠消化道吻合手术的质量直接与胰漏相关,胰漏往往是十二指肠切除术后腹腔出血启动点。经过多年外科学者探讨及临床总结,胰肠粘膜对接吻合方式作为主要胰肠吻合方式之一,在临床得到广泛应用,但胰腺粘膜与空肠粘膜对接吻合操作方法临床多种多样,尚没有统一的标准,操作不当,可能延误手术时间、导致局部组织出血及其它组织的副损伤影响胰肠吻合口愈合,轻度胰漏延期患者出院时间,重度胰漏则出现反复腹腔出血,严重时危及生命。有文献报道胰漏致死率高达20~50%[1]。
2.影响胰腺粘膜与空肠粘膜对接吻合操作的主要因素及容易出现的问题。①手术视野的暴露。胰腺脏器属于腹膜后器官,位置比较低且固定,如果开始吻合就将胰腺、空肠拉在一起缝合打结,任何缝合方法在有限的视野里均会显得比较困难,术者感到力不从心,不仅缝合速度慢,对胰肠吻合质量也不甚满意。如果患者肥胖,身体前后径较深,局部手术视野的暴露会更加困难。可能出现胰肠吻合质量不佳,出现胰漏。②胰腺残端后壁与肠系膜上静脉血管的显露。胰肠吻合无论哪一种方式,胰腺残端后壁及肠系膜上静脉的显露至关重要,胰腺后壁与肠管缝合操作时,如果显露不清很容易伤及肠系膜上静脉或分支静脉,引起局部出血,局部视野更加模糊,为吻合增加困难,更严重的是局部出血处理不当,可能因撕裂肠系膜上静脉导致更严重的大出血。反复的局部止血缝合,可能出现局部组织缺血、糜烂、缺乏生机。③胰腺组织质地。胰腺质地软硬、水肿程度也是影响胰肠吻合的重要因素。胰腺质地较软或水肿容易在缝合打结过程中切割胰腺组织,导致出血或缝合困难[2]。④缝合方式。如果手术视野暴露不充分、胰腺组织质脆,缝合方式不当,容易切割、撕裂胰腺组织或局部血管。⑤缝线的种类。由于胰腺及周围组织容易出血,相对粗糙的缝线容易摩擦胰腺组织,损伤胰腺组织,不利于胰肠吻合。
4. 分离式环形连续缝合行胰肠吻合的优点。①.吻合视野暴露清楚。该缝合方法为分离式缝合,开始吻合时,胰腺残端与空肠缝合间隔一定距离,胰腺后壁、周围血管、缝针的针距、缝合部位均暴露很清楚。避免了由于视野有限、胰腺后壁显露不清所造成的缝合不均、损伤周围血管情况。国内也有学者先将缝线穿好再打结,也是分离式缝合的一种体现[3]。②.不易切割胰腺组织。由于该方法是连续缝合,缝合完毕胰肠腹面后再收线,缝线力量分散,局部单针受力较小,不易切割胰腺组织。③.胰腺残端断面被肠管完整包埋。胰十二指肠切除术后腹腔出血,多数因为胰液或感染腐蚀导致胰腺残端面出血[4],该方法环形连续缝合,空肠肠壁紧贴于胰腺断面,并将胰腺断面完全严密包埋,避免局部胰漏或感染导致胰腺残端出血。本病案23例无一例出现吻合口出血。④.不需胰肠粘膜缝线吻合。典型的胰肠粘膜吻合,需要胰腺主胰管与空肠粘膜四点缝线吻合[5],本研究介绍方法由于胰腺残端与空肠粘膜对接紧密,胰管粘膜实际上已经与空肠粘膜紧密接触,不需要主胰管与空肠粘膜再单独缝线吻合。本病案43例均没有行空肠粘膜与胰管粘膜单纯吻合,仅有一例出现II级胰漏,胰漏原因不排除与该患者高龄(78岁)、手术创伤大(右半结肠切除联合胰十二指肠切除术)、体质相对较差、组织水肿等因素密切相关。4例出现I级胰漏,多考虑与针眼胰液渗出有关。因此,只要胰管能置入支撑管(支撑管直径根据胰管可选择),均能利用该吻合方式,不用担心胰管直径小于3mm,胰管粘膜与空肠粘膜吻合效果差的可能[6]。打破了因胰管过细(直径小于3mm),空肠粘膜与胰管粘膜吻合质量差的临床理念。⑤.缝合速度快。目前临床胰肠吻合未有固定的缝合方法、亦无标准的胰肠吻合起始时间,故本研究胰肠吻合时间无从对比分析长短,但由于该方法视野暴露清楚,局部出血少,缝合质量肯定,重复性缝合操作少,不需要空肠粘膜与胰管粘膜单独吻合,理论上该吻合方法明显缩短手术时间。
5. 分离式环形连续缝合行胰肠吻合需要注意事项。①.尽可能先行胰肠后壁缝合。先行胰肠后壁吻合收紧缝线后再行前壁吻合,避免缝线凌乱。②.连续缝合时尽可能缝线保持一定的张力,避免缝线凌乱。③.尽可能使用较细的无损伤滑线。无损伤滑线容易收紧线,对组织创伤小。
总之,随着外科学者对胰十二指肠切除手术的不断认识,胰肠吻合方式及操作方法也不断在改进,每个术者对不同的胰肠吻合方式及操作方法会有相应的感受及体会,选择不同的胰肠吻合方法及操作方式,分离式环形连续缝合行胰肠吻合方法虽然案例应用相对较少,吻合效果有待大宗病例进一步临床验证,但该方法理论上的优势为广大术者行胰十二指肠切除胰肠吻合方式及操作方法提供了一种新的思路。
参考 文献 略
