- 难治性结核性胸膜炎应用胸腔镜治疗临床分析
- 发布于 2014-11-24 20:47 来源:吕利征医生
结核性胸膜炎是常见的结核性疾病,以单侧或双侧胸膜腔不同程度积液为主要特征,在我国约占胸腔积液的半数。经全身抗结核及时抽液等治疗,大多可使胸水消失并治愈,但仍有部分患者虽经反复抽液置管引流及有效抗结核治疗仍不能控制,使积液分隔、呈多房小腔、包裹改变,胸腔积液难以吸收,形成难治性结核性胸膜炎。以往这类病人多数加以胸腔内给药,当胸膜肥厚并最终转化为脓胸时只能开胸胸膜剥脱,损伤大,愈后不理想。呼伦贝尔市第二人民医院胸外科吕利征
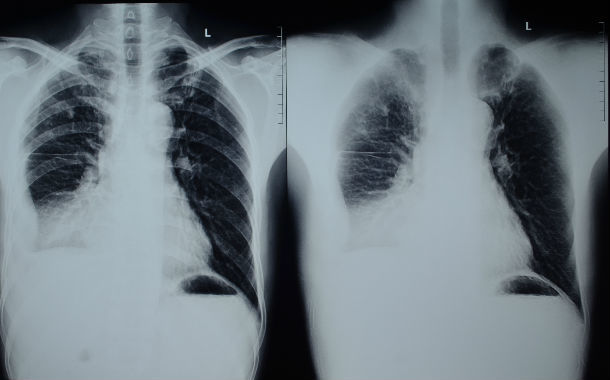
我们从2011年1月开始全麻下应用胸腔镜或辅助小切口治疗难治性结核性胸膜炎。选取2011年1月~2014年1月住院期间行胸腔镜治疗的30例患者。入组标准为: 发病时间小于2个月,反复穿刺及置胸腔闭式引流管引流不畅,胸部CT证实胸膜明显增厚胸液分隔包裹。男16例。女14例:年龄16~58岁,平均(39±12)岁。根据中华医学会结核病学分会制定的标准诊断为结核性胸腔积液,并按照全国结核病短程化疗协作组方案给予抗结核( 2HRZE/4HR) 及强的松,病程<1个月,经反复胸穿抽液或胸腔插管闭式引流有效抗结核药物和( 或) 口服糖皮质激素治疗,仍表现为中至大量胸腔积液或胸水呈包裹分隔胸部CT证实形成纤维板影响肺复张者。现总结报告如下:
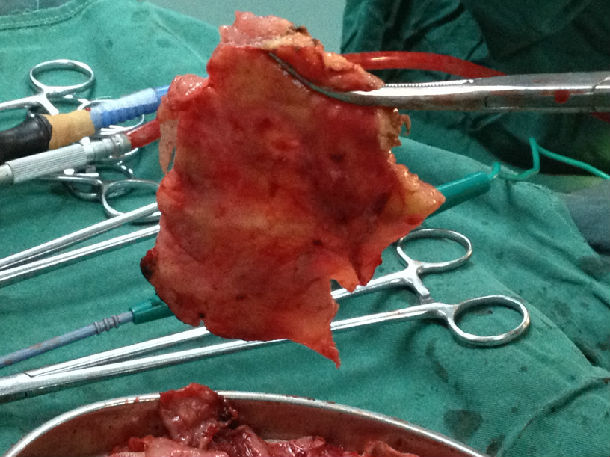
一 手术方法:
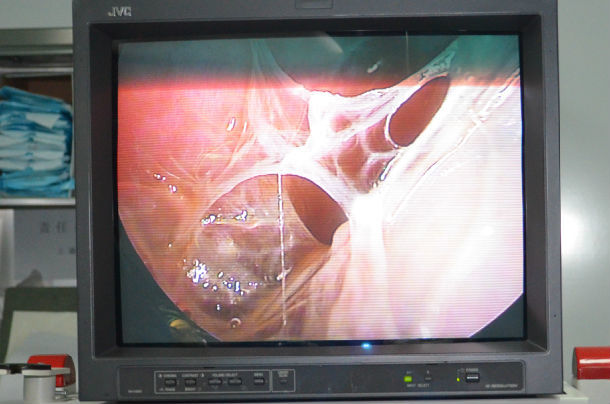
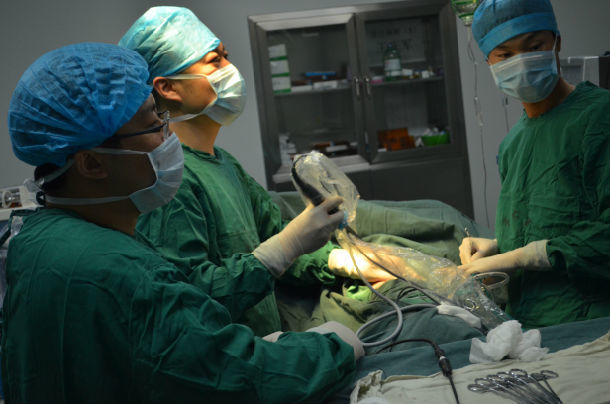
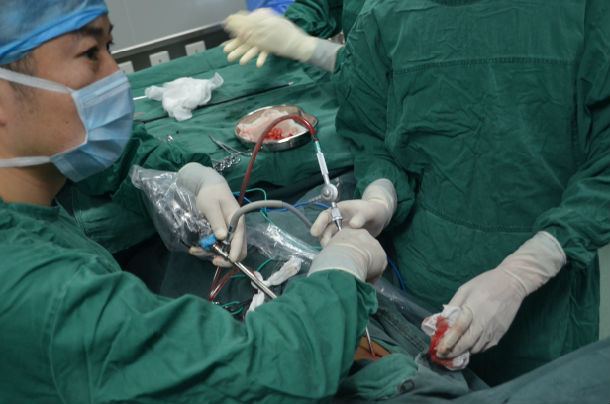
均采用全麻双腔气管插管,健侧卧位,根据术前超声定位,结合X线片,选择不同位置。一般选择在腋前线与腋后线之间第7、8肋间切口,长1.5cm,首先吸引出部分胸腔积液或干酪样物质,置入胸腔镜,行单孔操作处理积液将胸水包裹分隔打通,分离胸膜粘连带,剥离纤维板 再根据手术中情况,切开第二或第三操作孔,并可根据手术需要三孔置入器械可互换,插入电凝钩吸引器等,镜下见胸膜充血水肿,附着大量纤维素膜,部分呈脓性改变并可见大量的粘连带形成及胸膜肥厚,仔细剥离胸膜粘连带,打通分隔及剥除块摩擦,清除渗出的纤维素膜,吸净胸水,术中尽量剥除胸膜纤维板,放置胸腔闭式引流,向胸腔内注入冲洗液并患侧通气后可见肺组织表面漏气,大的漏气给予腔镜下缝合,小的漏气无需处理,术毕观察患侧肺复张情况。在第一个切口处放置引流管1根。通过对分组病人的干预过程、疗效、随访进行分析,组治疗效果。
二 结果:
手术均顺利完成,无严重并发症及围手术期死亡病例,手术操作时间40~160min,平均为( 65.5±26.2)
min 术中出血50~200ml,均未输血。术后胸腔闭式引流管放置时间4~9d,平均( 4.5±1.7) d 。;应用胸腔镜手术患者术后呼吸困难及胸闷明显缓解,经过积极的抗结核治疗,住院周期缩短,总体治疗费用较为手术难治性结核性胸膜炎患者减少,减轻了患者的经济负担。经术后随访3个月至2年了解到患者恢复良好,复发率极低,胸腔积液无复发病历,受压肺均复张理想,ct示胸膜厚度平均1.23±0.10mm,胸廓畸形加重仅1例,其余肋间隙松解增宽,肋间神经压迫性痛均缓解或消失。
三 讨论:
结核性胸膜炎是由结核菌及代谢产物进入正处于高度过敏状态的机体胸膜腔中所引起的胸膜炎症 当机体处于高度变态反应状态,结核菌及其代谢产物侵入胸膜,则引起渗出性胸膜炎 胸膜炎症早期先有胸膜充血水肿和白细胞浸润占优势,随后淋巴细胞转为多数,胸膜内皮细胞脱落,其表面有纤维蛋白渗出,继而浆液渗出,形成胸腔积液,胸膜常有结核性结节形成 病变多为单侧,胸膜腔内有数量不等的渗出液,一般为浆液性,偶见血性或化脓性。[1]目前国内结核性胸膜炎包裹性胸腔积液多采用有效抗结核基础上多次反复抽液治疗,有时加适量糖皮质激素以减少渗出。也有胸腔内注射尿激酶的方法目的是促进胸水吸收,经全身抗核及时抽液等治疗,大多可使胸水消失并治愈,有部分患者因胸膜粘连局限形成包裹,而包裹性积液内有大量纤维素样粘连形成分隔,胸水不宜抽出胸膜肥厚及包裹性胸腔积液的形成主要是渗出的大量纤维蛋白原形成纤维蛋白( 纤维素) , 覆盖于胸膜,随后纤维素机化发生纤维性粘连形成包裹胸腔积液不易消失,临床治疗困难。而且由于病程迁延,胸膜粘连增厚进行性加重,造成肺体积缩小,胸廓塌陷,肺功能受累 有研究发现约54%的结核性胸膜炎患者出现弥漫性胸膜肥厚,胸膜增厚是影响肺功能的独特危险因素。虽然日后部分患者能够接受纤维板剥脱手术,但是该手术偶然性较大,纤维板剥脱程度以及范围难以保障,术后胸腔残腔消除情况取决于肺膨胀程度 ,部分患者需要再次接受胸廓成形术,患者无论从身心健康方面还是经济方面均蒙受严重损失。
通过胸腔镜早期干预治疗结核性胸膜炎,术后呼吸困难及胸闷明显缓解,住院周期及抗结核用药时间缩短,复发率大大降低,无论从防止胸膜增厚还是消除胸腔残留积液方面均取得了满意的效果,有效减少了患者结核性脓胸形成,避免日后不得不实施创伤较大的胸膜剥脱等手术,同时也减轻了患者的经济负担。









